
【题目】最新研究表明,有毒气体H2S具有参与调节神经信号传递、舒张血管减轻高血压的功能。
(1)下列事实中,可以用来比较H2S与H2SO3的酸性强弱的是______(填标号)。
A.H2S 的还原性强于H2SO3
B.0.10 mol·L-1的H2S和H2SO3的pH分别为4.5和2.1
C.H2S 不能与NaHCO3溶液反应,而H2SO3可以
D.等浓度的两种溶液pH 值: NaHS > NaHSO3
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知(1)式和(5)式的热化学方程式分别为___________、________________,制得等量H2所需能量系统I是系统II的_______倍。
(3)H2S与CO2在高温下发生反应: H2S(g)+CO2(g) ![]() COS(g) +H2O(g) △H >0;保持T1温度,将0.20mol CO2与0.80mol H2S充入2.5L的空钢瓶中,反应平衡后COS的物质的量分数为0.02
COS(g) +H2O(g) △H >0;保持T1温度,将0.20mol CO2与0.80mol H2S充入2.5L的空钢瓶中,反应平衡后COS的物质的量分数为0.02
①H2S的平衡转化率a1=_______%,反应平衡常数K=______________。
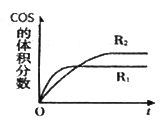
②在不同条件下发生上述反应,COS 的体积分数随时间(t)的变化如图所示,根据图象可以判断曲线R1、R2对应的下列反应条件中不同的是____________(填字母序号)CO2的转化率a2__a1,(填”>”或“<”)
A.压强 B.温度 C.催化剂
(4)反应开始,保持T1温度,2L 钢瓶中充入0.08molCO2、0.40mo1H2S、0.02molCOS和0.02molH2O,则此时V正___V逆(填”>”或“<”)判断依据是___________________________。
【答案】 BCD ![]() H2S(g)=H2(g)+S(s) ΔH=+20 kJ/mol 14.3倍 2.5 2.8×10–3 B > > Qc>K,向正反应方向进行
H2S(g)=H2(g)+S(s) ΔH=+20 kJ/mol 14.3倍 2.5 2.8×10–3 B > > Qc>K,向正反应方向进行
【解析】(1)A. 还原性与酸性强弱无关,故A错误;B.0.10 mol·L-1的H2S和H2SO3的pH分别为4.5和2.1,说明亚硫酸的电离程度大于氢硫酸,亚硫酸的酸性大于氢硫酸,故B正确;C.H2S 不能与NaHCO3溶液反应,而H2SO3可以说明亚硫酸的酸性大于碳酸大于氢硫酸,故C正确;D.越弱越水解,等浓度的两种溶液pH值: NaHS > NaHSO3,说明酸性亚硫酸大于氢硫酸,故D正确;故选BCD;
(2)系统(Ⅰ)涉及水的分解,系统(Ⅱ)涉及硫化氢的分解,利用盖斯定律分别将系统(Ⅰ)的(2)、(3)和H2O(l)=H2(g)+ ![]() O2(g) △H=+286kJ/mol处理得H2SO4(aq)=SO2(g)+ H2O(l)+
O2(g) △H=+286kJ/mol处理得H2SO4(aq)=SO2(g)+ H2O(l)+ ![]() O2(g) △H=+327kJ/mol;系统(Ⅱ)的(2)、(3)、(4)处理得H2S (g)=H2(g)+S(s) △H=+20kJ/mol;
O2(g) △H=+327kJ/mol;系统(Ⅱ)的(2)、(3)、(4)处理得H2S (g)=H2(g)+S(s) △H=+20kJ/mol;
根据系统I、系统II的热化学方程式可知:每反应产生1mol氢气,后者吸收的热量比前者少,所以制取等量的H2所需能量较少的是系统II,制得等量H2所需能量系统I是系统II的![]() =14.3倍,故答案为:H2SO4(aq)=SO2(g)+ H2O(l)+
=14.3倍,故答案为:H2SO4(aq)=SO2(g)+ H2O(l)+ ![]() O2(g) △H=+327kJ/mol;H2S (g)+=H2(g)+S(s)△H=+20kJ/mol;14.3倍;
O2(g) △H=+327kJ/mol;H2S (g)+=H2(g)+S(s)△H=+20kJ/mol;14.3倍;
(3)对于反应H2S(g)+CO2(g)![]() COS(g)+H2O(g)
COS(g)+H2O(g)
起始(mol) 0.800.20 0 0
转化(mol) x x x x
平衡(mol) 0.80-x0.20-x x x
反应平衡后COS的物质的量分数为0.02,则![]() =0.02,x=0.02。
=0.02,x=0.02。
①H2S的平衡转化率a1=![]() ×100%=2.5%,体积为2.5L,则平衡时各物质的浓度为c(H2S)=
×100%=2.5%,体积为2.5L,则平衡时各物质的浓度为c(H2S)= ![]() mol/L=0.312mol/L,c(CO2)
mol/L=0.312mol/L,c(CO2) ![]() mol/L=0.072mol/L,c(COS)=c(H2O)=
mol/L=0.072mol/L,c(COS)=c(H2O)= ![]() mol/L=0.008mol/L,则K=
mol/L=0.008mol/L,则K=![]() =0.00285≈2.8×10–3,故答案为:2.5;2.8×10–3;
=0.00285≈2.8×10–3,故答案为:2.5;2.8×10–3;
②A.该反应前后气体的物质的量不变,改变压强,平衡不移动,错误;B.改变温度,平衡移动发生移动,正确;C.改变催化剂,平衡不移动,错误;故选B;升高温度,化学平衡向吸热反应方向移动,因此平衡向正反应方向移动,H2S的转化率增大,即a2>a1,故答案为:B;>;
(4)反应开始,保持T1温度,2L钢瓶中充入0.08molCO2、0.40mo1H2S、0.02molCOS和0.02molH2O,此时Qc= =
=![]() =0.0125>K=0.00285,反应向正反应方向进行,V正>V逆,故答案为:>;Qc >K,向正反应方向进行。
=0.0125>K=0.00285,反应向正反应方向进行,V正>V逆,故答案为:>;Qc >K,向正反应方向进行。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】常温下,将HC1气体通入到1L浓度均为0.1mol/L的NaA和NaB的混合溶液中,混合溶液的pH与离子浓度变化的关系如图所示(忽略溶液体积的变化)。下列叙述不正确的是

A. Ka(HB)的数量级为10-9
B. 酸性的强弱顺序为HCl>HA>HB
C. 当通入0.1molHC1气体时,c(B-)>c(A-)
D. 当混合溶液呈中性时,c(Na+)=c(Cl-)+c(A-)+c(B-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼是动植物所必须的微量元素,其单质和化合物广泛应用于冶金、机械、化工、核工业、医药、农业等部门。利用硼镁矿(主要成分为Mg2B2O3·5H2O)制取制硼酸、金属镁及粗硼的工艺流程图如下:

已知:①硼砂为Na2B4O7·10H2O
②硼酸(H3BO3)是一种可溶于水的一元弱酸,与过量的NaOH反应生成Na[B(OH)4]
③硼酸在不同温度下的溶解度:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度(g/100g水) | 3 | 3 | 5 | 7 | 9 | 11 | 15 | 18 | 23 | 29 |
(1)粉碎硼铁矿的目的是:______________;Mg2B2O5·H2O中B的化合价为:______价。
(2)滤渣的主要成分是: ________
(3)硼酸的电子式: ________;写出硼酸在水中电离的方程式: ________________;
(4)X为硼酸晶体加热完全脱水后的产物,其与Mg反应制取粗硼的化学方程式为: ________;
(5)硼砂溶于90℃热水后,常用稀硫酸调pH至2~3(酸性)制取HBO3晶体,该反应的离子方程式为: ________________;从上述溶液中获得H3BO3晶体的操作: ________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实脸室取等物质的量的KClO3分别发生下述反应: 反应一:有催化剂存在时,受热分解得到氧气;
反应二:不使用催化剂,加热至743K左右,得到KClO4和KCl.
下列关于①和②的说法正确的是( )
A.两个反应中都只有一种元素化合价发生改变
B.两个过程生成KCl的物质的量相同
C.发生氧化反应的元素相同
D.发生还原反应的元素相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某小组同学在烧杯中加入5mL1.0mol/L盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,如图A所示,该反应是_________________________。(填“吸热”或“放热”)反应,其能量变化可用图中的____________(填“B”或“C”)表示。

(2)已知拆开1mo1H-H键、1molN![]() N、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。当1mo1 NH3_______________(填“放出”或“吸收”)________kJ 的热量。
N、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。当1mo1 NH3_______________(填“放出”或“吸收”)________kJ 的热量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D 同族,C的简单离子和B的简单离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物中阴阳离子的个数比为1:1。回答下列问题:
(1)五种元素中,原子半径最大的是____________(填元素名称),非金属性最强元素的是___________。
(2)由元素A分别和元素B、D、E所形成的共价型化合物中,热稳定性最差的是
______________(用化学式表示)。
(3)元素A和E形成的化合物与元素A和B形成的化合物反应,产物的电子式为_________________,其中存在的化学键类型为_________________________。
(4)E离子的结构示意图是____________________;
元素D最高价氧化物的水化物的化学式为_________________。
(5)单质E与水反应的离子方程式为 ____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有下列4种离子的溶液中加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
A. NO3- B. Ba2+ C. OH- D. Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com