
 Na2S2O3ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬Ņ×ČÜÓŚĖ®£®ŌŚÖŠŠŌ»ņ¼īŠŌ»·¾³ÖŠĪČ¶Ø£®
Na2S2O3ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬Ņ×ČÜÓŚĖ®£®ŌŚÖŠŠŌ»ņ¼īŠŌ»·¾³ÖŠĪČ¶Ø£®·ÖĪö £Ø1£©Įņ·ŪÄŃČÜÓŚĖ®”¢Ī¢ČÜÓŚŅŅ“¼£¬ŅŅ“¼ŹŖČóæÉŅŌŹ¹Įņ·ŪŅ×ÓŚ·ÖÉ¢µ½ČÜŅŗÖŠ£»
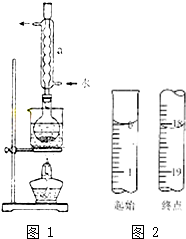
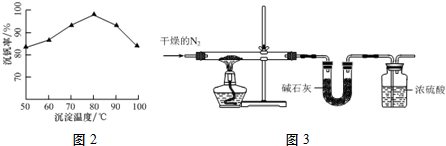
£Ø2£©øł¾ŻŅĒĘ÷½į¹¹ĢŲÕ÷Š“³öĘäĆū³Ę£¬ĄäÄż¹ÜĘšµ½ĄäÄż»ŲĮ÷µÄ×÷ÓĆ£»
£Ø3£©ÓÉÓŚNa2S2O3”¢Na2SO3¾ßÓŠ»¹ŌŠŌ£¬Ņ×±»ŃõĘųŃõ»ÆNa2SO4£¬¼ģŃéČÜŅŗŹĒ·ńĮņĖįøłĄė×Ó½ųŠŠÅŠ¶Ļ£»
£Ø4£©S2O32-ÓėĒāĄė×ÓŌŚČÜŅŗÖŠÄܹ»·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉĮņµ„ÖŹÓė¶žŃõ»ÆĮņ£»
£Ø5£©µĪ¶ØĒ°ČÜŅŗĪŖĪŽÉ«£¬µĪ¶Ø½įŹųŗ󣬵āµ„ÖŹŹ¹µķ·Ū±äĄ¶£»
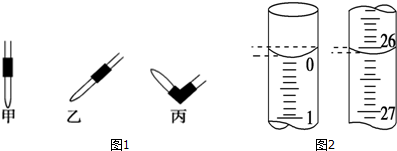
£Ø6£©øł¾ŻĶ¼Ź¾µÄµĪ¶Ø¹ÜÖŠŅŗĆę¶Į³ö³õ¶ĮŹż”¢ÖÕ¶ĮŹż£¬Č»ŗó¼ĘĖć³öĻūŗĵāµÄ±ź×¼ČÜŅŗĢå»ż£»
½ųŠŠ¹żĮæ¼ĘĖć£¬øł¾Ż²»×ćĮæµÄĪļÖŹ¼ĘĖćĄķĀŪ²śĮ棬øł¾Ż·“Ó¦2S2O32-+I2ØTS4O62-+2I-£¬æÉÖŖn£ØS2O32-£©=2n£ØI2£©£¬½ų¶ų¼ĘĖćѳʷµÄ²śĀŹ£»
£Ø7£©Na2S2O3»¹ŌŠŌ½ĻĒ棬ŌŚČÜŅŗÖŠŅ×±»Cl2Ńõ»Æ³ÉSO42-£¬·“Ӧɜ³ÉĮņĖįÄĘ”¢ĀČ»ÆÄĘ£¬ÅäĘ½ŹéŠ“Ąė×Ó·½³ĢŹ½£®
½ā“š ½ā£ŗ£Ø1£©Įņ·ŪÄŃČÜÓŚĖ®Ī¢ČÜÓŚŅŅ“¼£¬ĖłŅŌĮņ·ŪŌŚ·“Ó¦Ē°ÓĆŅŅ“¼ŹŖČóŹĒŹ¹Įņ·ŪŅ×ÓŚ·ÖÉ¢µ½ČÜŅŗÖŠ£¬
¹Ź“š°øĪŖ£ŗŹ¹Įņ·ŪŅ×ÓŚ·ÖÉ¢µ½ČÜŅŗÖŠ£»
£Ø2£©øł¾ŻĶ¼Ź¾ÖŠŅĒĘ÷µÄ½į¹¹ĢŲÕ÷£¬æÉÖŖŅĒĘ÷aĪŖĄäÄż¹Ü£¬øĆŹµŃéÖŠĄäÄż¹Ü¾ßÓŠĄäÄż»ŲĮ÷µÄ×÷ÓĆ£¬
¹Ź“š°øĪŖ£ŗĄäÄż¹Ü£»ĄäÄż»ŲĮ÷£»
£Ø3£©ÓÉÓŚNa2S2O3”¢Na2SO3¾ßÓŠ»¹ŌŠŌ£¬Ņ×±»ŃõĘųŃõ»ÆNa2SO4£¬ĖłŅŌæÉÄÜ“ęŌŚµÄŌÓÖŹŹĒNa2SO4£»¼ģŃéĮņĖįÄʵķ½·ØĪŖ£ŗȔɣĮæ²śĘ·ČÜÓŚ¹żĮæĻ”ŃĪĖį£¬¹żĀĖ£¬ĻņĀĖŅŗÖŠ¼ÓBaCl2ČÜŅŗ£¬ČōÓŠ°×É«³Įµķ£¬Ōņ²śĘ·ÖŠŗ¬ÓŠNa2SO4£¬
¹Ź“š°øĪŖ£ŗNa2SO4£» ȔɣĮæ²śĘ·ČÜÓŚ¹żĮæĻ”ŃĪĖį£¬¹żĀĖ£¬ĻņĀĖŅŗÖŠ¼ÓBaCl2ČÜŅŗ£¬ČōÓŠ°×É«³Įµķ£¬Ōņ²śĘ·ÖŠŗ¬ÓŠNa2SO4£»
£Ø4£©S2O32?ÓėĒāĄė×Ó·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³Éµ»ĘÉ«Įņµ„ÖŹ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗS2O32?+2H+=S”ż+SO2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗS2O32?+2H+=S”ż+SO2”ü+H2O£»
£Ø5£©µĪ¶Ø½įŹųŗ󣬵āµ„ÖŹŹ¹µķ·Ū±äĄ¶£¬ĖłŅŌµĪ¶ØÖÕµćŹ±ČÜŅŗŃÕÉ«±ä»ÆĪŖ£ŗÓÉĪŽÉ«±äĪŖĄ¶É«£¬
¹Ź“š°øĪŖ£ŗÓÉĪŽÉ«±äĪŖĄ¶É«£»
£Ø6£©øł¾ŻĶ¼Ź¾µÄµĪ¶Ø¹ÜÖŠŅŗĆęæÉÖŖ£¬µĪ¶Ø¹ÜÖŠ³õŹ¼¶ĮŹżĪŖ0£¬µĪ¶ØÖÕµćŅŗĆę¶ĮŹżĪŖ18.10mL£¬ĖłŅŌĻūŗĵāµÄ±ź×¼ČÜŅŗĢå»żĪŖ18.10mL£»
øł¾Ż·“Ó¦2S2O32-+I2ØTS4O62-+2I-æÉÖŖ£¬n£ØS2O32-£©=2n£ØI2£©£¬ĖłŅŌW g²śĘ·ÖŠŗ¬ÓŠNa2S2O3•5H2OÖŹĮæĪŖ£ŗ0.1000 mol•L-1”Į18.10”Į10-3L”Į2”ĮM=3.620”Į10-3Mg£¬Ōņ²śĘ·µÄ“æ¶ČĪŖ£ŗ$\frac{3.620”Į1{0}^{-3}Mg}{Wg}$”Į100%=$\frac{3.620”Į1{0}^{-3}Mg}{Wg}$”Į100%£¬
¹Ź“š°øĪŖ£ŗ18.10£»$\frac{3.620”Į1{0}^{-3}Mg}{Wg}$”Į100%£»
£Ø7£©Na2S2O3»¹ŌŠŌ½ĻĒ棬ŌŚČÜŅŗÖŠŅ×±»Cl2Ńõ»Æ³ÉSO42-£¬ÅäĘ½ŗóµÄĄė×Ó·½³ĢŹ½ĪŖ£ŗS2O32?+4Cl2+5H2O=2SO42?+8Cl?+10H+£¬
¹Ź“š°øĪŖ£ŗS2O32?+4Cl2+5H2O=2SO42?+8Cl?+10H+£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧŹµŃéÖʱø£¬Éę¼°ŅĒĘ÷Ź¶±š”¢Ąė×ӵļģŃé·½·Ø”¢¶Ō×°ÖĆ·ÖĪöĘĄ¼Ū”¢Ńõ»Æ»¹Ō·“Ó¦µĪ¶ØÓė¼ĘĖć”¢Ąė×Ó·½³ĢŹ½ŹéŠ“µČ£¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĶßĖ¹ÖŠ¼×ĶéŗĶŃõĘųµÄÖŹĮæ±ČĪŖ1£ŗ4Ź±¼«Ņ×±¬ÕØ£¬“ĖŹ±¼×ĶéÓėŃõĘųµÄĢå»ż±ČĪŖ1£ŗ2 | |
| B£® | ÓūÅäÖĘ1.00 L1.00 mol•L-1µÄNaClČÜŅŗ£¬æɽ«58.5 g NaClČÜÓŚ1.00 LĖ®ÖŠ | |
| C£® | 22.4LN2ŗĶH2µÄ»ģŗĻĘųĢåÖŠŗ¬NAøöŌ×Ó | |
| D£® | 3molµ„ÖŹFeĶźČ«×Ŗ±äĪŖFe3O4£¬µĆµ½8NAøöµē×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃ鱹ŗÅ | NaOHČÜŅŗµÄÅØ¶Č£Ømol•L-1£© | µĪ¶ØĶź³ÉŹ±£¬NaOHČÜŅŗµĪČėµÄĢå»ż£ØmL£© | “ż²āŃĪĖįµÄĢå»ż£ØmL£© |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
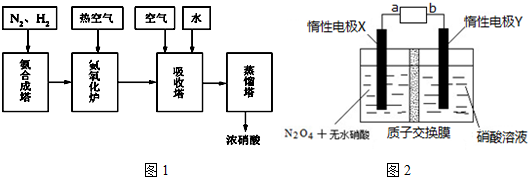
 ÓĆŅŃÖŖÅØ¶ČµÄNaOHČÜŅŗ²ā¶ØijH2SO4ČÜŅŗµÄÅØ¶Č£¬²Īæ¼ČēĶ¼£¬“ÓĻĀ±ķÖŠŃ”³ö
ÓĆŅŃÖŖÅØ¶ČµÄNaOHČÜŅŗ²ā¶ØijH2SO4ČÜŅŗµÄÅØ¶Č£¬²Īæ¼ČēĶ¼£¬“ÓĻĀ±ķÖŠŃ”³ö| ׶ŠĪĘæÖŠµÄŅŗ | µĪ¶Ø¹ÜÖŠµÄČÜŅŗ | Ń”ÓĆÖøŹ¾¼Į | Ń”ÓƵĪ¶Ø¹Ü | |
| ¢Ł | ¼ī | Ėį | ŹÆČļ | £ØŅŅ£© |
| ¢Ś | Ėį | ¼ī | ·ÓĢŖ | £Ø¼×£© |
| ¢Ū | ¼ī | Ėį | ·ÓĢŖ | £Ø¼×£© |
| ¢Ü | Ėį | ¼ī | ·ÓĢŖ | £ØŅŅ£© |
| A£® | ¢Ł¢Ś | B£® | ¢Ł¢Ū | C£® | ¢Ś¢Ü | D£® | ¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

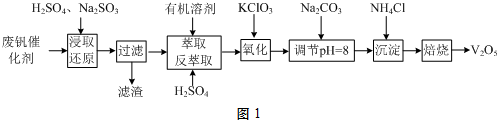
| A£® | ²½Öč1ĪŖĪüČČ·“Ó¦£¬²½Öč2ĪŖ·ÅČČ·“Ó¦ | |
| B£® | E2£¾E3£¾E1 | |
| C£® | 1mol C·¢ÉśøĆ·“Ó¦Ź±ĪüŹÕµÄÄÜĮæĪŖE3-E1 | |
| D£® | E2-E1£¼E2-E3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com