
【题目】检验SO2气体中是否混有CO2气体,可采用的方法是( )
A. 通过品红溶液
B. 通过澄清石灰水
C. 先通过氢氧化钠溶液,再通过澄清石灰水
D. 先通过酸性高锰酸钾溶液,再通过澄清石灰水
科目:高中化学 来源: 题型:
【题目】涂改液是一种使用率较高的工具,实验证明涂改液含有苯的同系物和卤代烃。下列说法中不正确的是
A. 涂改液危害人体健康、污染环境 B. 中学生最好不用或慎用涂改液
C. 苯的同系物和卤代烃皆可溶于水 D. 苯的同系物和卤代烃是涂改液中的溶剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表前四周期的一部分,下列叙述正确的是( )

A. Y单质在空气中燃烧生成YO3
B. Z元素的最高价氧化物的水化物酸性最强
C. X的氢化物为H2X
D. Y、Z和W的阴离子半径依次增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO·SiO2, 还含少量Fe2O3、A12O3、SiO2等杂质)通过如下方法制取。
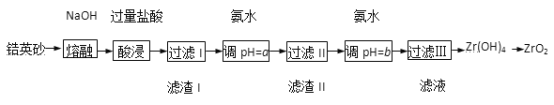
已知:ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
(1)在熔融时NaOH和ZrSiO4发生反应的化学方程式为________________,滤渣I的化学式为_______。
(2)用氨水调pH=a是为了使滤液I的杂质离子_______(填离子符号)完全沉淀,而ZrO2+不沉淀;继续加氨水至pH=b时,所发生反应的离子方程式为____________________________。
(3)过滤III所得滤液含有NH4Cl,向其中加入CaCO3粉末并加热,可得到两种气体。该反应的离子方程式为_______________。
(4)为得到纯净的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E 都含X元素,其转化关系如下图所示。
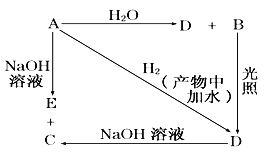
(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):
A _____,B _____,C ______,D_____,E___________。
(2)写出下列反应的化学方程式:
A+H2O:______________;
A+NaOH:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列方法测定某水样中O2的含量。
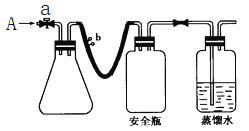
(1)实验原理
①用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为_____________________________。
②在酸性条件下,再用I-将生成的MnO(OH)2,还原为Mn2+,反应的离子方程式为_____________________________。然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为I2+2 Na2S2O3=2Na1+Na2S4O6。
(2)实验步骤
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是___________________________;
②用注射器抽取某水样20. 00mL从A处注入锥形瓶;
③再分别从A处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸;
⑥重复④的操作;
⑦取下锥形瓶,向其中加入23滴_______作指示剂;
⑧用0.005 mol L -1 Na2S2O3溶液滴定至终点。滴定终点的现象是___________________________。
(3)数据分析
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________ mg L-1。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将_________ (填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯气通入到水中所发生反应的化学方程式为______________________。已知生成物之一是一种弱酸,试写出该物质在水溶液中的电离方程式______________。某同学将有色布条浸泡在新制的氯水中,发现布条很快被漂白。对此他认为可能是因为氯水中含有某种粒子使布条褪色,于是他提出如下的假设,请你帮他设计实验方案以验证他的假设。
编号 | 假设原因 | 验证方案 |
1 | 可能是因为Cl2分子 | A:_____________ |
2 | 可能是因为H+ | B:_____________ |
3 | 可能是因为Cl- | C:_____________ |
4 | 可能是因为HClO | ———————————————— |
5 | 可能是因为ClO- | D:_____________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.氧化镁熔点很高,可作为优质的耐高温材料
B.有色玻璃就是某些胶态金属氧化物分散于玻璃中制成
C.溴化银可用于感光材料,也可用于人工降雨
D.分子筛可用于物质分离,还能作干燥剂和催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对分子中σ键重叠方式的分析不正确的是
A | B | C | D |
H2 | HCl | Cl2 | ClF |
两个氢原子的s轨道重叠 | 氢原子的s轨道和氯原子的p轨道重叠 | 一个氯原子的s轨道和另一个氯原子的p轨道重叠 | 氯原子的p轨道和氟原子的p轨道重叠 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com