
 ��
��
���� ̽������Һ��ķ�Ӧ������Һ���������������������������屽���廯�⣬���ɵ��屽������ˮ���ܶȱ�ˮ��Ϊ���ɫ��������NaOH��Һ��ȥ�����屽�е�Һ�壬�˷�ӦΪ���ȷ�Ӧ�����ɵ�HBr���б����壬���ñ���ȥHBr�л��е����ʣ�Cװ�ã�������ʯ����Һ����HBr�����ˮ��Һ�����ԣ�Dװ�ã����������������Br-�Ĵ��ڣ�Eװ�ã�������NaOH����β����Fװ�ã�����HBr�����ܽ���ˮ����Ӧ�����Ϸ�����ְ�����β������ʱ��Ҫ���������ݴ˷������⣮
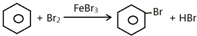
��1������Һ����Fe�Ĵ������·���ȡ����Ӧ�����屽���廯�⣻
��2���屽�е����ӷ����Ǽ��Է��ӵ����������ڷǼ��Է��ӵ��ܼ����ݴ˷����������ã�
��3���屽���л������������������Һ�����ܶȴ�������������Һ��
��4������©�������θ�����ܷ�ֹ��Һ������
��5���������巢����ȡ����Ӧ����Ӧ�����廯�����ɣ��廯������ˮ�õ������ᣬ��������ʹʯ����Һ���ɫ���������ܺ���������Ӧ���ɵ���ɫ�����廯����
��� �⣺��1��Fe���巴Ӧ�����廯���������巢��ȡ����Ӧ�����屽��HBr���л���ѧ����ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��2���屽�е����ӷ�����ͱ����ǷǼ��Է��ӣ�������������ԭ��֪���������ڱ������Ա���������������������
�ʴ�Ϊ����ȥHBr�л��е�Br2��
��3���屽���л������������Һ����������屽������������Һ�����ܣ����屽���ܶȴ���ˮ���ܶȣ�������B�е�����������Һ��ɹ۲쵽�������ǵײ������״Һ�壬
�ʴ�Ϊ����Һ�ײ�����ɫ�͵Σ�
��4��������ѹ������ѹ���仯ʱ��Һ��������������DEװ���е����ܲ�������Һ�п��Է�ֹ���������õ�©���¿ںܴ�Һ��������С�ĸ߶Ⱦ��кܴ�������������Һ��ı�����ѹ�����ɵͳ�ѹ���IJ����⣬��������ϲ����п������룬Һ�岻�ᵹ�����϶˵�ϸ�ܵ������Ծ��з��������õ�������DEF��
�ʴ�Ϊ��DEF��
��5���������ӳɷ�Ӧ����Ӧ�����廯�����ɣ��廯������ˮ�õ������ᣬ���������������ʣ���ʹʯ����Һ���ɫ���������ܺ���������Ӧ���ɵ���ɫ�����廯�������Թ۲�D��E���Թܣ�������������D�Թ�����ɫʯ����Һ������죬���ڵ��ܿ��а���������E���г���dz��ɫ��������˵�������巢����ȡ����Ӧ�����Ǽӳɷ�Ӧ��
�ʴ�Ϊ��D��ʯ�����E�в�������ɫ������
���� ���⿼���˱���ȡ����Ӧʵ�飬�����֪ʶ���з�Ӧ����ʽ����д��������жϼ����ʣ��ۺ��Խ�ǿ��������Ӧԭ���ǽ��Ĺؼ�����Ŀ�Ѷ��еȣ�


 ���ʿ��ÿ��ֳɳ�ϵ�д�
���ʿ��ÿ��ֳɳ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�30 g���������������еĹ��ۼ���ĿΪ6NA | |
| B�� | ��״���£�0.4 g D2���������ӵ���ĿΪ0.2NA | |
| C�� | �����£�1 L pH=12�İ�ˮ��Һ�к���NH4+��ĿΪ0.01NA | |
| D�� | ��״���£�ʢ��11.2 L NO2���ܱ������е�ԭ����Ϊ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
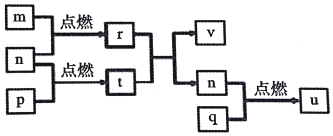 ����������Ԫ��X��Y��Z��W��ԭ������������������Ԫ���γɵĵ�������Ϊm��n��p��q��r��t��u����ЩԪ����ɵĶ�Ԫ���������uΪ�γ��������Ҫ����֮һ��25��ʱ��0.01mol•L-1��v��Һ�У�$\frac{c��O{H}^{-}��}{c��{H}^{+}��}$=1.0��1010���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
����������Ԫ��X��Y��Z��W��ԭ������������������Ԫ���γɵĵ�������Ϊm��n��p��q��r��t��u����ЩԪ����ɵĶ�Ԫ���������uΪ�γ��������Ҫ����֮һ��25��ʱ��0.01mol•L-1��v��Һ�У�$\frac{c��O{H}^{-}��}{c��{H}^{+}��}$=1.0��1010���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ԭ�Ӱ뾶�Ĵ�С��W��Z��Y��X | |
| B�� | Z�ֱ���Y��W��ɵĻ������л�ѧ�����Ϳ�����ͬ | |
| C�� | v������ˮ�ĵ����u�ܴٽ�ˮ�ĵ��� | |
| D�� | ճ��q���Թܿ��þƾ�ϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ��ͼ��ʾ��������A�е�Ũ����μӵ�ʢ��MnO2����ƿ�У����Ⱥ��������������ͨ��װ��B��C��Ȼ����ͨ�����ȵ�ʯӢ������D�����������ۣ�����ش�
��ͼ��ʾ��������A�е�Ũ����μӵ�ʢ��MnO2����ƿ�У����Ⱥ��������������ͨ��װ��B��C��Ȼ����ͨ�����ȵ�ʯӢ������D�����������ۣ�����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ﵽƽ��ʱA����ת����Ϊ40% | B�� | �ﵽƽ��ʱc��B��Ϊ1.0mol•L-1 | ||
| C�� | �ﵽƽ��ʱc��B��=2c��D�� | D�� | �ﵽƽ��ʱc��D��Ϊ0.5mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� | �� | |
| A | ���������� | ֻ��AgBr�������� |
| B | ���ɵ���ɫ���� | AgCl��AgBr�������У���AgCl�������� |
| C | ���������� | AgCl��AgBr����������AgCl�������� |
| D | ���ɻ�ɫ���� | AgCl��AgBr�������У���AgBr�������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
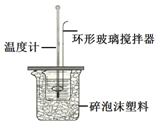 �ⶨϡ�����ϡ���������к��ȵ�ʵ��װ����ͼ��ʾ�����к��ȣ���ϡ��Һ�У��������кͷ�Ӧ����1molˮʱ�ķ�Ӧ�ȣ�
�ⶨϡ�����ϡ���������к��ȵ�ʵ��װ����ͼ��ʾ�����к��ȣ���ϡ��Һ�У��������кͷ�Ӧ����1molˮʱ�ķ�Ӧ�ȣ�| �¶� ʵ������� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | |
| HCl | NaOH | ||
| 1 | 26.1 | 26.1 | 29.3 |
| 2 | 25.9 | 25.9 | 29.0 |
| 3 | 26.3 | 26.3 | 29.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ�����������������Ϊ������ʱ�ɷų��������� | |
| B�� | �������������н�ȡ��ͨ���������ȡ����ű���������� | |
| C�� | ����Ʒ������Ʒ���ճ������б��㷺Ӧ������Ϊ������Ϊ���ý��� | |
| D�� | ���õ�Ư�۱�������ΪƯ��������е�O2��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com