
【题目】在某一容积为2 L的密闭容器中加入0.6molH2O(g)和0.4molCO,在一定条件下发生如下反应:CO(g) + H2O(g )![]() CO2(g) + H2(g)
CO2(g) + H2(g)
(1)若反应2min后,容器中CO仅剩0.2mol,则0~2min间CO的平均反应速率为___。
(2)该反应为放热反应,若升高温度,化学反应速率___;CO的转化率___。(填“增大”、“减小”或“不变”)。
科目:高中化学 来源: 题型:
【题目】根据下列实验:
①向Fe2(SO4)3和CuSO4的混合液中加入过量铁粉,充分反应,有红色固体析出,过滤。
②取①中滤液,向其中滴加KSCN溶液,观察现象。
判断下列说法正确的是
A. 氧化性Cu2+>Fe3+
B. ①中所得固体只含铜
C. ①中滤液含有Cu2+和Fe2+
D. ②中不会观察到溶液变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对溴苯乙烯与丙烯的共聚物E是一种高分子阻燃剂,具有低毒、热稳定性好等优点.由烃A合成E的路线如图所示.
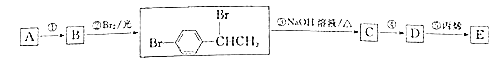
回答下列问题:
(1)![]() 的名称 ______ ;
的名称 ______ ;![]() 的反应条件 ______ .
的反应条件 ______ .
(2)共聚物E的结构简式 ______ .
(3)反应![]() 的化学方程式 ______
的化学方程式 ______ ![]() 反应
反应![]() 的化学方程式 ______ .
的化学方程式 ______ .
(4)满足下列条件的C的同分异构体的结构简式 ______ ![]() 任写一种
任写一种![]() .
.
![]() 能使
能使![]() 溶液呈紫色
溶液呈紫色 ![]() 核磁共振氢谱显示有3组峰面积比为6:2:1.
核磁共振氢谱显示有3组峰面积比为6:2:1.
(5)丙烯催化二聚得到2,![]() 二甲基
二甲基![]() 丁烯,F与2,
丁烯,F与2,![]() 二甲基
二甲基![]() 丁烯互为同分异构体,且所有碳原子处于同一平面,写出F的结构简式 ______ .
丁烯互为同分异构体,且所有碳原子处于同一平面,写出F的结构简式 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.6倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.6倍,下列叙述正确的是
A.A的转化率变小B.平衡向正反应方向移动
C.D的体积分数变大D.a>c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A与![]() 、CO形成B,B能发生银镜反应,C分子中只有一种氢,相关物质转化关系如下
、CO形成B,B能发生银镜反应,C分子中只有一种氢,相关物质转化关系如下![]() 含有相同官能团的有机物通常具有相似的化学性质
含有相同官能团的有机物通常具有相似的化学性质![]() :
:
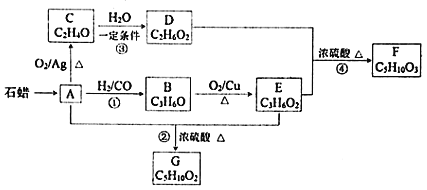
请回答:
![]() 有机物C的结构简式是______,反应②的反应类型是______。
有机物C的结构简式是______,反应②的反应类型是______。
![]() 写出一定条件下发生反应①的化学方程式______。
写出一定条件下发生反应①的化学方程式______。
![]() 下列说法不正确的是______
下列说法不正确的是______![]() 填字母
填字母![]() 。
。
A.化合物A属于烃
B.化合物D含有两种官能团
C.用金属钠无法鉴别化合物F、G
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞![]() 是治疗轻、中度急性脑缺血的药物,合成J的一种路线如下
是治疗轻、中度急性脑缺血的药物,合成J的一种路线如下

已知:![]()
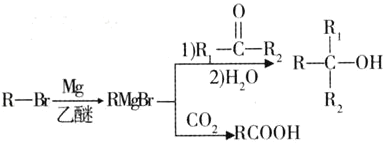
![]() 的核磁共振氢谱只有一组峰;
的核磁共振氢谱只有一组峰;
![]() 能发生银镜反应;
能发生银镜反应;
![]() 是一种酯,分子中除苯环外还含有一个五元环。
是一种酯,分子中除苯环外还含有一个五元环。
![]() 苯环上的卤原子在常压下遇到NaOH的溶液很难水解。
苯环上的卤原子在常压下遇到NaOH的溶液很难水解。
回答下列问题:
![]() 中官能团的名称:________、________。
中官能团的名称:________、________。
![]() 的系统命名是________;J的结构简式为________。
的系统命名是________;J的结构简式为________。
![]() 由A生成B的化学方程式为________,反应类型为________。
由A生成B的化学方程式为________,反应类型为________。
![]() 与新制的氢氧化铜悬浊液反应的化学方程式为________。
与新制的氢氧化铜悬浊液反应的化学方程式为________。
![]() 在一定条件下生成高分子化合物的结构简式为________。
在一定条件下生成高分子化合物的结构简式为________。
![]() 的同分异构体中核磁共振氢谱有4组峰且能与
的同分异构体中核磁共振氢谱有4组峰且能与![]() 溶液发生显色反应,任写出其中两种符合上述条件的同分异构体的结构简式________。
溶液发生显色反应,任写出其中两种符合上述条件的同分异构体的结构简式________。
![]() 由甲醛、化合物A与液溴为原料经下列步骤可得到
由甲醛、化合物A与液溴为原料经下列步骤可得到![]() 苯基乙醇。
苯基乙醇。
![]()
反应条件1为________;反应条件2所选择的试剂为________;L的结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。
N2+3H2![]() 2NH3
2NH3
现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生,下列有关说法正确的是( )
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应的速率都为零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅在地壳中的含量较高。硅及其化合物的开发由来已久,在现代生活中有广泛应用。回答下列问题:
(1)1810年瑞典化学家贝采利乌斯在加热石英砂、木炭和铁时,得到一种“金属”。这种“金属”可能是_______。
(2)陶瓷、水泥和玻璃是常用的硅酸盐材料。其中,生产普通玻璃的主要原料有_______。
(3)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
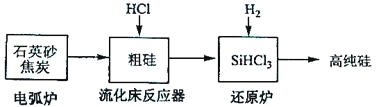
发生的主要反应 | |
电弧炉 | SiO2+2C |
流化床反应器 | Si+3HCl |
还原炉 | SiHCl3+H2 |
①用石英砂和焦炭在电弧炉中高温加热也可以生产碳化硅,该反应的化学方程式为_______;碳化硅又称_______,其晶体结构与_______相似。
②在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,有关物质的沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和_______。
物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
③SiHCl3极易水解,其完全水解的产物为_______。
(4)氯碱工业可为上述工艺生产提供部分原料,这些原料是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是
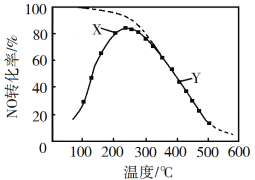
A. 反应2NO(g)+O2(g)![]() 2NO2(g)的ΔH>0
2NO2(g)的ΔH>0
B. 图中X点所示条件下,延长反应时间能提高NO转化率
C. 图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D. 380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡转化率为50%,则平衡常数K>2000
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com