
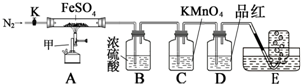
 �����������壨FeSO4•7H2O���׳��̷������������»�ֽ⣮ij��ѧ�о�С��������ͼװ��̽��FeSO4�ֽ��IJ��
�����������壨FeSO4•7H2O���׳��̷������������»�ֽ⣮ij��ѧ�о�С��������ͼװ��̽��FeSO4�ֽ��IJ��| ʵ�� | �ζ��ܿ�ʼ���� | �ζ��յ���� |
| 1 | 0 | 19.98 |
| 2 | 0.10 | 20.12 |
| 3 | 0 | 20.16 |
���� ��ͼ��װ����������ʡ�Լг������������װ�õ������ԣ�ȷ��ȡm gFeSO4��������Ӳ�ʲ������У���E�еĵ��ܳ���ˮ�ۣ�����K��ͨ��һ��ʱ���N2���رջ���K������A�еIJ�����һ��ʱ���E�е�������ˮ�ۼ���ƿ���ռ����������壬�ô����ǵ�ľ������E�����ռ������壬�����ǵ�ľ���ܹ���ȼ��֤��������������A�й��岻�ٷֽ��ֹͣ���ȣ���K������ͨ�뵪������������ȴ���õ�����ɫ��ĩ˵���ֽ����������������������Ԫ�ػ��ϼ�һ���н��͵�����SO2������ԭ���غ�͵����غ�����ж����ɲ����л�Ӧ����������������ͨ��װ��B��Ũ����������������װ��C�и��������Һ���ն�������װ��D��Ʒ����Һ����֤���������Ƿ������װ�ã����װ��E�ռ��زĵ��������м��飬
��1��װ��ͼ��������Ϊ�ƾ���ƣ�
��2��B��Ũ������������շֽ������SO3��
��3��ʵ������з���C����Һ��ɫ��dz��D�������Ա仯˵�������������������Һȫ�����շ���������ԭ��Ӧ��
��4��ͨ��һ��ʱ��N2��ԭ���ǽ�װ���ڲ�����������������װ��2��ȫ���գ�
��5���ٸ��������Һ���Ϻ�ɫ��������ᷢ��������ԭ��Ӧ����Ӧ�յ�������ݸ��������Һ��ɫ�жϣ�
3��ʵ���������ϴ���ȥ������1��2��������Һ���=$\frac{19.98+20.12-0.1}{2}$=20ml��n��H2C2O4��=0.20mol/L��0.020L=0.004mol��
2KMnO4+5H2C2O4+3H2SO4�TK2SO4+2MnSO4+10CO2��+8H2O
2 5
n 0.040mol
n=0.0016mol��
װ��C�й���ʣ�����������ʵ���=0.0016mol��$\frac{100}{20}$=0.008mol�����������Ӧ�ĸ���������ʵ���=0.020L��1.00mol/L-0.008mol=0.012mol��
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+��
5 2
n��SO2�� 0.012mol
n��SO2��=0.03mol
����Bװ����ʵ��ǰ������0.80gΪ��������n��SO3��=$\frac{0.80g}{80g/mol}$=0.01mol
��Ԫ�ؽ������ɶ����������ת��0.03mol��2=0.06mol��
ԭ���غ�õ���Ӧ��FeSO4��0.03mol+0.01mol=0.04mol��
2FeSO4 ��Fe2O3��2e-
2 1 2
0.04mol 0.02mol 0.04mol
FeSO4��O2��4e-
1 4
0.005mol 0.02mol
��Ӧ��FeSO4��Fe2O3��SO3��SO2��O2=0.04��0.002��0.01��0.012��0.005=8��4��2��6��1
�ݴ���д��ѧ����ʽ��
��6������������Ƿ���δ�ֽ���������������ʵ�����ʣ��������Ƿ��������ӣ����뼸��K3[Fe��CN��6]��Һ��������������ɫ����֤�����������ӣ�
��� �⣺��1��װ��ͼ��������Ϊ�ƾ���ƣ�
�ʴ�Ϊ���ƾ���ƣ�
��2��̽��FeSO4�ֽ��IJ������ݷ�����֪���ֽ�����������������������ɣ����������ԭ��Ӧ��Ԫ�ء���Ԫ�ػ��ϼ����ߣ�����Ԫ�ػ��ϼ۽������ɶ�������ԭ���غ�ɵõ�ͬʱ������������������B��Ũ������������շֽ������SO3��
�ʴ�Ϊ�����շֽ������SO3��
��3��ʵ������з���C����Һ��ɫ��dz��D�������Ա仯˵�������������������Һȫ�����գ���Ӧ�����ӷ���ʽΪ��5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+��
�ʴ�Ϊ��5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+��
��4��FeSO4��ȫ�ֽ����Ҫͨ��һ��ʱ��N2��ԭ���ǽ�װ���ڲ�����������������װ��2��ȫ���գ�ͬʱ��ֹ����������
�ʴ�Ϊ����װ���ڲ�����������������װ��2��ȫ���գ�ͬʱ��ֹ����������
��5��ȷ��ȡ20.00mL��Һ����ƿ�У���������ϡ�����ữ����0.20mol/L��H2C2O4��Һ�ζ����յ㣬�ǵζ�װ��C��ʣ�������أ�
�ٸ��������Һ���Ϻ�ɫ��������ᷢ��������ԭ��Ӧ����Ӧ�յ�������ݸ��������Һ��ɫ�жϣ��������һ����Һ�Ϻ�ɫ�仯Ϊ��ɫ�Ұ�����ޱ仯֤����Ӧ�ﵽ�յ㣬
�ʴ�Ϊ����Һ���Ϻ�ɫ��Ϊ��ɫ�Ұ���Ӳ��ָ����Ϻ�ɫ��
��3��ʵ���������ϴ���ȥ������1��2��������Һ���=$\frac{19.98+20.12-0.1}{2}$=20ml��n��H2C2O4��=0.20mol/L��0.020L=0.004mol��
2KMnO4+5H2C2O4+3H2SO4�TK2SO4+2MnSO4+10CO2��+8H2O
2 5
n 0.040mol
n=0.0016mol��
װ��C�й���ʣ�����������ʵ���=0.0016mol��$\frac{100}{20}$=0.008mol�����������Ӧ�ĸ���������ʵ���=0.020L��1.00mol/L-0.008mol=0.012mol��
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+��
5 2
n��SO2�� 0.012mol
n��SO2��=0.03mol
����Bװ����ʵ��ǰ������0.80gΪ��������n��SO3��=$\frac{0.80g}{80g/mol}$=0.01mol
��Ԫ�ؽ������ɶ����������ת��0.03mol��2=0.06mol��
ԭ���غ�õ���Ӧ��FeSO4��0.03mol+0.01mol=0.04mol��
2FeSO4 ��Fe2O3��2e-
2 1 2
0.04mol 0.02mol 0.04mol
FeSO4��O2��4e-
1 4
0.005mol 0.02mol
��Ӧ��FeSO4��Fe2O3��SO3��SO2��O2=0.04��0.002��0.01��0.012��0.005=8��4��2��6��1
��Ӧ�Ļ�ѧ����ʽΪ��8FeSO4$\frac{\underline{\;����\;}}{\;}$4Fe2O3+2SO3��+6SO2��+O2����
�ʴ�Ϊ��8FeSO4$\frac{\underline{\;����\;}}{\;}$4Fe2O3+2SO3��+6SO2��+O2����
��6������������Ƿ���δ�ֽ���������������ʵ�����ʣ��������Ƿ��������ӣ�����������ӵ����������Լ��ͷ�Ӧ������ƣ����岽��Ϊ������Һ��Ĺ���ת�Ƶ�С�ձ��У���������ˮ������ˣ�ȡ������Һ���Թ��У����뼸��K3[Fe��CN��6]��Һ��������������ɫ������˵����������δȫ���ֽ⣬��֮��ֽ���ȫ��
�ʴ�Ϊ������Һ��Ĺ���ת�Ƶ�С�ձ��У���������ˮ������ˣ�ȡ������Һ���Թ��У����뼸��K3[Fe��CN��6]��Һ��������������ɫ������˵����������δȫ���ֽ⣬��֮��ֽ���ȫ��
���� ���⿼���˷�Ӧ����ķ����жϡ�ʵ������з�Ӧ����Ͳⶨ�������ζ�ʵ����������ͼ��㣬��Ҫ��������ԭ��Ӧ�����غ�ļ������ϻ�ѧ����ʽ�����ջ����ǽ���ؼ�����Ŀ�ѶȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ۢ� | B�� | �٢� | C�� | �ڢ� | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
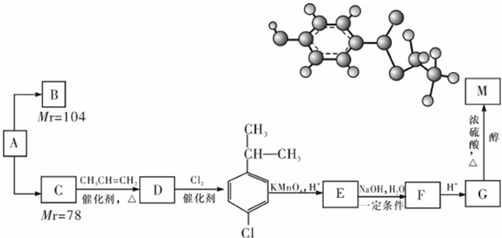
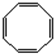 ��
��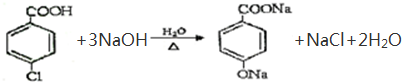 ��
�� ��
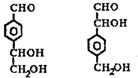
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
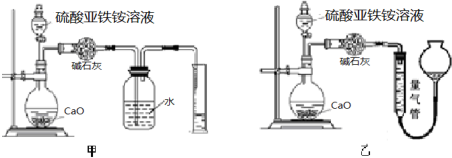
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ҵ����������ˮ�ࡢƯ�ۣ�����Ҫ��ʯ��ʯΪԭ�� | |
| B�� | ij��ˮ��Ʒ����һ��ʱ���PH��4.68��Ϊ4.00������Ϊˮ���ܽ��CO2���� | |
| C�� | �ڽ����·�������Σ�����������ˮ������ѧ��Ӧ�ų�������������ʹ��ѩ�ڻ� | |
| D�� | ���������Դ�����ô��¿��Է�Ϊ����ʱ���������Դ����ʯ��Դ������Դʱ����Ŀǰ��ȫ������Ҫ���ڶ���Դʱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ǿˮ����������ˮ | B�� | ��ǿˮ������������ | ||
| C�� | ��ǿˮ�����ܾ���ǿ�����ԡ�ǿ���� | D�� | ��ǿˮ��������������������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�Ľṹ��ʽCH2CH2 | B�� | NaCl�ĵ���ʽ  | ||
| C�� | CO2���ӵĽṹʽO-C-O | D�� | Mgԭ�ӽṹʾ��ͼ 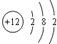 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.5mol�� | B�� | 1mol���� | C�� | 1mole- | D�� | 1mol�Ȼ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com