
����Ŀ������ʥ·��˹��ѧ������һ�����͵��Ҵ���أ�������(H+)�ܼ�����200������ʱ���硣����ܷ�ӦΪ��C2H5OH +3O2��2CO2+3H2O�����ʾ������ͼ������˵����ȷ����

A. a��Ϊ��ص�����
B. ��ع���ʱ������b���ص��߾������ٵ�a��
C. ��������ĵ缫��ӦΪ��4H+ + O2+ 4e��2H2O
D. ��ع���ʱ��1mol�Ҵ�������ʱ����6mol����ת��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʵ���г�����Һ���Լ������ữ�������ữ�����Ĵ�ʩ��ȷ����(����)
A.������Һ�Ƿ���SO![]() ʱ���������Ὣ��������Һ�ữ��Ȼ�������еμ�BaCl2��Һ
ʱ���������Ὣ��������Һ�ữ��Ȼ�������еμ�BaCl2��Һ
B.Ϊ��߸��������Һ�����������������Ὣ���������Һ�ữ
C.������Һ���Ƿ���Fe3��ʱ���������ữ
D.���Լ���SO![]() ����BaCl2��Һ��HNO3�ữ
����BaCl2��Һ��HNO3�ữ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ԫ��aA��bB��cC��dD��eE��ԭ�ӽṹʾ��ͼ�ֱ�Ϊ
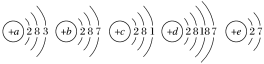
��ش��������⣺
(1)����ͬ���ڵ�Ԫ����________(��Ԫ�ط��ţ���ͬ)������ͬ�����Ԫ����________��
(2)��������ǿ��Ԫ����________���ǽ�������ǿ��Ԫ����________��
(3)����Ԫ��������������Ӧ��ˮ���������ǿ����________(�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:��NH3����ԭNOxʱ�������·�Ӧ.
��Ӧ��:4NH3 (g)+6NO(g) ![]() 5N2(g)+6H2O(l) H1=-1 807. 0 kJ��mol��1,
5N2(g)+6H2O(l) H1=-1 807. 0 kJ��mol��1,
��Ӧ��:4NH3(g)+6NO2(g) ![]() 5N2(g)+3O2(g)+6H2O(l) H2=?
5N2(g)+3O2(g)+6H2O(l) H2=?
��Ӧ��:2NO(g)+O2(g) ![]() 2NO2(g) H3=-113.0kJ��molһ1
2NO2(g) H3=-113.0kJ��molһ1
(1)��Ӧ�ڵ�H2==_____________��
(2)Ϊ̽���¶ȼ���ͬ�����Է�Ӧ�ٵ�Ӱ��.�ֱ��ڲ�ͬ�¶ȡ���ͬ������.����������ʼ���������ظ�ʵ��.����ͬʱ���ڲ��N2Ũ�ȵı仯�������ͼ��ʾ��

�ٷ�Ӧ�ٵ�ƽ�ⳣ���ı���ʽK=________����ͬ�¶���.�ڴ����������·�Ӧ��ƽ�ⳣ��______(����ڡ���С�ڡ����ڡ�)�ڴ����ҵ������·�Ӧ��ƽ�ⳣ����
��N���N2Ũ�ȼ�С��ԭ�������_____________________��
(3)ij�¶��£���1 L�����ܱ������г�ʼͶ��4 mol NH3��6 mol NO������Ӧ��.�����������ʵ���Ϊ7.5molʱ��Ӧ�ﵽƽ��.��NH3��ת����Ϊ____����ƽ������ʱ��Ϊ5 min.����NO��ʾ�˷�Ӧ0��5 min�ڵ�ƽ����Ӧ����Ϊ______.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������ȷ���ǣ� ��
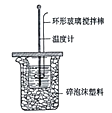
A. ����ͼ��ʾ�Dzⶨ�к��ȵļ���װ�ã���С���ձ�����������ĭ���ϵ������ǹ̶�С�ձ�
B. ����50 mL 0.55 mol��L-1������������Һ���ֱ���50 mL 0.50 mol��L-1�������50 mL0.50 mol��L-1�������ַ�Ӧ������Ӧ�ⶨ���к��Ȳ����
C. ʵ��ʱ��Ҫ��¼��ʼ�¶�T1������¶�T2
D. ��һ��ʵ����ݹ�ʽ���ɵó��кͷ�Ӧ�ķ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO��H2��һ�������¿��Ժϳ��Ҵ���2CO(g) + 4H2(g)![]() CH3CH2OH(g) + H2O(g)�����������У���˵��������Ӧ��һ��������һ���ﵽ����ȵ���
CH3CH2OH(g) + H2O(g)�����������У���˵��������Ӧ��һ��������һ���ﵽ����ȵ���
A. COȫ��ת��Ϊ�Ҵ�
B. ��4NA��H-H����ͬʱ������46g�Ҵ�
C. ����Ӧ�ں��º����ܱ������н��У������л��������ܶȲ��ٸı�
D. ����Ӧ�ھ��Ⱥ����ܱ������н��У��������¶Ȳ��ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ش��������⣺
(1)2 mol CO(NH2)2�к�_____molNԭ��, ����Oԭ������________g H2O������ԭ������ȡ�
(2)12.4 g Na2R��Na��0.4 mol����Na2R��Ħ������Ϊ_______����R������Ϊ1.6 g��Na2R�������ʵ���Ϊ_________��
(3)CO��CO2�Ļ������18 g���ڱ�״���µ����Ϊ11.2 L�����������ƽ��Ħ������Ϊ________�����������CO������Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��������߽�����ȷ����(����)
A.����һ�����ʵ���Ũ�ȵ���Һʱ������ƿ����ྻ�����ʹ��ǰ��Ҫ�����Ƿ�©ˮ
B.ʵ��������100.0 g��20%���Ȼ�����Һ����ȡ20.0 g��NaCl���ձ��У��ټ���80.0 mL��ˮ����ֽ����
C.ʵ��������Ҫ480 mL 2.0 mol��L��1������������Һ��������Һʱ�ȳ����������ƹ���38.4 g��Ȼ���ٰ����ܽ⡢��ȴ����Һ�����ݡ�ҡ�ȵȲ�����в���
D.ʵ��������500 mL 0.2 mol��L��1������������Һ������ڳ���ʱ�������������������ŷ�(������������ȷ)����������ҺŨ�Ȼ�ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪʵ������ȡ���ռ������������������������������̽����ʵ��װ��ͼ��

��1����Ӧǰ����__��װŨ����(��д��������)��__��װMnO2(��д��������)��
��2��װ��A����װ�Լ���__��Ŀ��__��װ��B����װ���Լ���___��Ŀ��__��
��3��װ��D����װ�Լ���__��������Ӧ�Ļ�ѧ����ʽΪ__��
��4��ʵ������ȡCl2�Ļ�ѧ����ʽ___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com