
由单质镁制硝酸镁的下列4个方案中,你认为可行而且符合“绿色化学”要求的方案是( )
A.Mg Mg(NO3)2
Mg(NO3)2
B.Mg MgCl2
MgCl2 Mg(OH)2
Mg(OH)2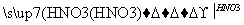 Mg(NO3)2
Mg(NO3)2
C.Mg MgO
MgO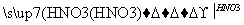 Mg(NO3)2
Mg(NO3)2
D.Mg MgSO4
MgSO4 Mg(NO3)2
Mg(NO3)2
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:
已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。回答下列问题:
(1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是 ;
(2)Q的具有相同化合价且可以相互转变的氧化物是 ;
(3)R和Y形成的二元化合物中,R呈现最高化合价的化合物的化学式是 ;
(4)这5个元素的氢化物分子中,①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式) ,其原因是 ;
②电子总数相同的氢化物的化学式和立体结构分别是 ;
(5)W和Q所形成的结构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCL气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数K=2.25。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
H2O(g)+CO(g)的平衡常数K=2.25。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A.反应开始时,反应速率:甲<乙<丙
B.平衡时,甲中和丙中H2的转化率均是
 60%
60%
C.平衡时,c(CO2)丙=2c(CO2)甲
D.平衡时,乙中CO2的体积分数大于60%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列选用的相关仪器、用品不符合实验要求的是( )
| A | B | C | D |
| 准确量取19.01 mL水 | 新制氯 | 测定0.1 mol/L Na2CO3溶液的pH |
|
| 25 mL酸式滴定管 | 带玻璃塞的棕色细口瓶 | 镊子、pH试纸、表面皿 | 分液漏斗、烧杯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下面所列的是中学化学实验室中几种常见的玻璃仪器:
①温度计 ②容量瓶 ③滴定管 ④烧杯 ⑤圆底烧瓶 ⑥量筒 ⑦玻璃棒
(1)在仪器上标明具体使用温度的是(不考虑温度计)________(填写编号);可作反应容器并可加热的是________(填写编号)。
(2)需要用温度计的实验是________(填写编号)。
①石油分馏 ②浓硫酸稀释 ③测定硝酸钾的溶解度
(3)玻璃棒的作用主要有以下三种。不同实验中其作用可能不完全相同,请回答下列问题:
①搅拌 ②引流 ③蘸取溶液
A.在“用无水碳酸钠配制100 mL 0.12 mol·L-1的碳酸钠溶液”的实验中,玻璃棒的作用是________(填写编号)。
B.在“用氢氧化钠溶液、碳酸钠溶液、氯化钡溶液、盐酸、水等试剂除去粗盐中的Mg2+、Ca2+、SO 等杂质离子以获得纯净的食盐”的实验中玻璃棒的作用可能是________(填写编号)。
等杂质离子以获得纯净的食盐”的实验中玻璃棒的作用可能是________(填写编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室里用铁屑、氧化铜、稀硫酸为原料制备铜,有下列两种途径:
(1)Fe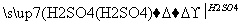 H2
H2 Cu
Cu
(2)CuO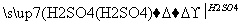 CuSO4
CuSO4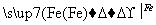 Cu
Cu
若用这两种方法制得等量的铜,则下列有关说法符合实际情况的是( )
A.消耗铁的质量不同
B.消耗硫酸的质量相同
C.生成硫酸亚铁的质量相同
D.消耗氧化铜的质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
关于乙酸的下列说法不正确的是
( )
A.乙酸是一种重要的有机酸,是具有强烈刺激性气味的液体
B.乙酸分子中含有四个氢原子,所以乙酸是四元酸
C.无水乙酸又称冰醋酸,它是纯净物
D.乙酸易溶于水和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A(C10H20O2)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。已知:

①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有________(选填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称依次是__________、____________。
(3)写出与D、E具有相同官能团的同分异构体的可能的结构简式:________________________________________________________________。
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2甲基1丙醇和甲酸在一定条件下制取E。该反应的化学方程式是______________________________________________________________
________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是一种重要的化工原料。工业上常用反应3Cl2+8NH3===N2+6NH4Cl检验氯气管道是否漏气。根据材料中的反应回答下列问题:
(1)氧化剂是________,还原剂是________。
(2)氧化剂与被氧化的还原剂分子个数比为________。
(3)当有68 g NH3参加反应时,被氧化的物质为______g,生成的还原产物为________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com