
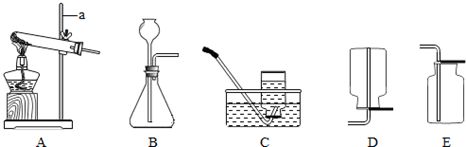
| ||
| ||
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
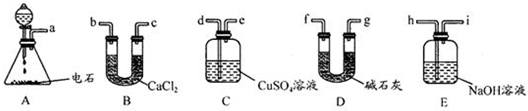
| HBr |
| 催化剂 |
| 操作a |
| NaOH溶液 |
| △ |
| 操作b |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | ||
| Z | W | M |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、定容后,又重新加水至刻度线 |
| B、烧杯和玻璃棒的溶液未转入容量瓶中 |
| C、定容时,眼睛俯视刻度线 |
| D、容量瓶洗净后没有干燥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com