
反应 A+B→C 的反应速率方程式为:v=k c(A)•c(B),v为反应速率,k为速率常数.当c(A)=c(B)=1mol/L时,反应速率在数值上等于速率常数.下列说法正确的是()
A. 只增大c(A)时,v也增大 B. 只增大c(A)时,v值不变
C. 只升高温度时,k值不变 D. 只升高温度时,k值变小
考点: 化学平衡的影响因素.
专题: 化学平衡专题.
分析: v与c(A)、c(B)成正比,无论只增大c(A)、只增大c(B)或同时增大c(A)、c(B),v均增大.若只升高温度,v增大,c(A)、c(B)不变,所以k值变大.
解答: 解:A.v与c(A)、c(B)成正比,只增大c(A),v增大,故A正确;
B.v与c(A)、c(B)成正比,只增大c(A),v增大,故B错误;
C.若只升高温度,v增大,c(A)、c(B)不变,所以k值变大,故C错误;
D.若只升高温度,v增大,c(A)、c(B)不变,所以k值变大,故D错误,
故选:A.
点评: 本题考查化学反应速率,难度不大,以信息题的形成考查,对学生的自学能力、分析能力有较好的考查.


科目:高中化学 来源: 题型:
下列说法中,正确的是()
A. 放热反应的发生均无需加热
B. 需要加热后才能发生的反应均是吸热反应
C. 伴有能量变化的物质变化都是化学变化
D. 物质发生化学反应都伴随着能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在反应2MnO4﹣+5H2S+6H+=2Mn2++5S↓+8H2O中,电子转移总数为10e﹣还原剂为H2S还原产物为 ,当反应中有80gS析出时,有 mol MnO4﹣被还原
(2)“绿色试剂”双氧水可作为采矿业废液消毒剂,如果要消除采矿业废液中的氰化物(如KCN),化学反应方程式为:KCN+H2O2+H2O=KHCO3+NH3↑.
①反应中发生氧化反应的物质为 ;
②H2O2被称为绿色氧化剂的理由是 .
③用单线桥表示出该反应电子转移的方向和数目:KCN+H2O2+H2O=KHCO3+NH3↑
查看答案和解析>>
科目:高中化学 来源: 题型:
在其他条件不变时,改变某一条件对反应:A2(g)+3B2(g)⇌2AB3(g)化学平衡状态的影响,得到如图变化规律(图中T表示温度,n表示物质的量),根据图示可得出的结论正确的是()

A. 正反应一定是放热反应
B. 达到平衡时A2的转化率大小为:b>a>c
C. 若T2>T1,则正反应一定是吸热反应
D. b点时,平衡体系中A、B原子数之比可能接近1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
模型法是化学中把微观问题宏观化的最常见方法,对于2HBr(g)⇌H2(g)+Br2(g)反应.下列四个图中可以表示该反应在一定条件下为可逆反应的是()
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
将经过酸洗除锈的铁钉,用饱和食盐水浸泡后放入如图所示装置中,下列叙述正确的是()
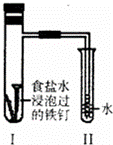
A. 过一段时间,Ⅱ试管中的导管内水柱上升
B. Ⅰ试管中铁钉由于发生电解反应而被腐蚀
C. 铁钉在该装置中被腐蚀的情况随时间的延长而加快
D. Ⅰ试管中铁钉发生反应的一个电极反应式为:2Cl﹣﹣2e﹣═Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
T1℃时,向一体积不变的密闭容器中加入1mol A、2mol B和0.5mol C三种气体发生反应,各物质浓度随时间变化如图一所示,其中c(C)的变化未画出来,但t1时刻c(C)=c(D);图二为t2时刻后改变反应条件,A的转化率与温度、压强的关系
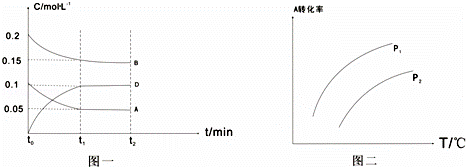
(1)t1=5min,则t0~t1阶段以C的浓度变化表示反应速率为v(C)= ,该反应的化学方程式为
(2)根据图二分析,温度升高,该反应的平衡常数将增大(填“增大”“减小”或“不变”),压强P1 P2 (填“>”“<”或“=”)
(3)若上述反应在T1℃、恒压下进行,A的转化率会减小(填“增大”“减小”或“不变”)
(4)在相同条件下(T1℃时,体积不变的密闭容器中),若起始时容器中加入2molD、 molB和 molC,才能达到t1时刻同样的平衡.
查看答案和解析>>
科目:高中化学 来源: 题型:
有一固体粉末,可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验.
(1)将该粉末溶于水得无色溶液和白色沉淀;
(2)在滤出的沉淀中加入稀硝酸,部分沉淀溶解,同时产生无色气体;
(3)取滤液做焰色反应,可以看到黄色火焰,透过蓝色钴玻璃片,观察不到紫色火焰.由上述现象可推断( )
|
| A. | 可能有Na2CO3 | B. | 一定有Na2SO4 | C. | 一定无NaCl | D. | 一定有K2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
2(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是 .
(2)肼﹣空气燃料电池是一种碱性燃料电池,电解质溶液是KOH溶液.肼﹣空气燃料电
池放电时:正极的电极反应式是 ;负极的电极反应式是 .
(3)如图是一个电化学过程示意图.假设使用肼﹣空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标标准状况下的空气 L(假设空气中氧气体积含量为20%)
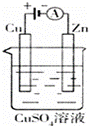
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com