
分析 已知①N2(g)+2O2(g)═N2O4(g),△H=+8.7kJ/mol;
②N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534.7kJ/mol;
利用盖斯定律将②×2-①可得2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g),并以此计算反应热.
解答 解:已知①N2(g)+2O2(g)═N2O4(g),△H=+8.7kJ/mol;
②N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534.7kJ/mol;
利用盖斯定律将②×2-①可得2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g),
△H=(-534.7kJ/mol)×2-(+8.7kJ/mol)=-1078.1kJ/mol,
故答案为:2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g)△H=-1078.1kJ•mo1-1.
点评 本题考查反应热的计算,题目难度不大,注意盖斯定律的应用,易错点为B,注意反应热与系数成正比.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:选择题
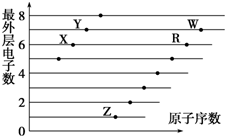
| A. | X和R在同一主族 | |
| B. | 含氧酸酸性:W>R | |
| C. | X与W可以形成酸性氧化物 | |
| D. | X、Z形成的化合物中可能含有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Ca2+、NO3-、CO32- | B. | Fe3+、K+、OH-、SO42- | ||
| C. | Ag+、Na+、Cl-、K+ | D. | K+、Na+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
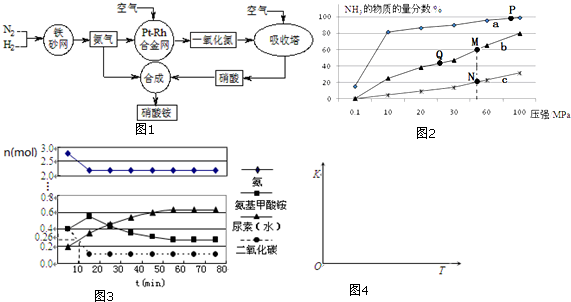
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠和稀盐酸 | B. | 金属钠和硫酸铜溶液 | ||
| C. | 金属镁和硫酸铜溶液 | D. | 铝粉和氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | |
| C | D |
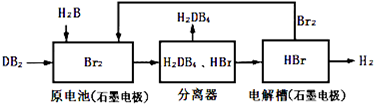
| 化学键 | H-H | Br-Br | H-Br |
| 键能(kJ/mol) | 436 | 194 | 362 |
| 化学式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
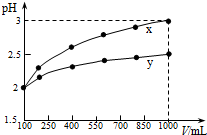
| A. | x为强酸,y为弱酸 | |
| B. | 稀释前x、y的物质的量浓度相等 | |
| C. | 随着稀释的进行,y的电离程度减小 | |
| D. | 等体积的x、y分别与足量的锌反应,y放出的氢气多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com