
【题目】(10分)某化学探究小组用如下实验证明了烧碱与稀硫酸能发生中和反应。
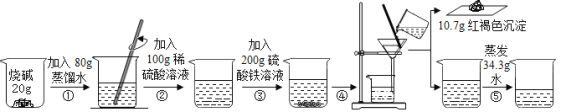
②③两步均充分反应,加入硫酸铁溶液,立即产生明显现象,最终得到只含一种溶质的无色溶液.请回答下列问题:
(1)①根据发生的反应及现象可知反应②结束时溶液中的离子有_____________(填离子符号);②无明显现象,发生反应的化学方程式是_____________;
(2)求解③中参加反应的烧碱的质量为_____________;
(3)发生中和反应的硫酸的物质的量为_____________ ;
(4)最终得到的无色不饱和溶液只含一种溶质,则所得溶液中溶质的质量分数为_____________。
【答案】(1)①Na+、OH-、SO42-;②H2SO4+2NaOH=Na2SO4+2H2O;
(2)12g;
(3)0.1mol;
(4)10%。
【解析】
试题分析:(1) ①根据发生的反应2NaOH+H2SO4=Na2SO4+2H2O可知及加入硫酸铁溶液会产生红褐色沉淀,说明碱过量,实验反应②结束时溶液中的离子有:Na+、OH-、SO42-;②硫酸与氢氧化钠发生酸碱中和反应,产生硫酸钠和水,反应的化学方程式是:H2SO4+2NaOH=Na2SO4+2H2O;(2)设与硫酸铁反应的氢氧化钠的质量为x,生成的硫酸钠的质量为y;
Fe2(SO4)3+6NaOH=3Na2SO4+2Fe(OH)3 ↓
240 426 214
x y 10.7g
214÷240=10.7g÷x,解得x=12g;426÷214=y÷10.7g,解得y=21.3g;反应开始有NaOH质量是20g,所以发生反应③消耗的NaOH的质量是20g-12g=8g;(3)硫酸与NaOH发生中和反应:2NaOH+ H2SO4= Na2SO4+2H2O,反应的NaOH的质量是20g-12g=8g,其物质的量是n(NaOH)=8g÷40g/mol=0.2mol,根据反应方程式可知硫酸的物质的量是n(H2SO4)=1/2 n(NaOH)=0.1mol;(4)设氢氧化钠与硫酸反应生成的硫酸钠的质量为z,
2NaOH+H2SO4=Na2SO4+2H2O
80 142
8g z
80÷142=8g÷z,解得 z=14.2g;因此最终得到的无色不饱和溶液中溶质的质量分数=
[(21.3g+14.2g)÷(20g+80g+100g+200g10.7g34.3g)]×100%=10%。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某有机物a的分子式和己烷相同,且主链上有4个碳原子,则下列关于a 的观点正确的是( )
A.a分子中可能有三个甲基
B.a的一氯代物可能有三种
C.a的分子式为C6H10
D.a能与溴的四氯化碳溶液发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是A、B两种物质的溶解度曲线,下列说法不正确的是( )

A.A物质的溶解度随温度升高而增大
B.t2℃时,A物质的溶解度大于B物质的溶解度
C.A的饱和溶液温度越高,溶质质量分数越大
D.t1℃时,A、B两种物质饱和溶液的质量分数为25%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)某无色溶液样品中溶质可能含有NaOH和Na2SO4,某化学小组同学为了确认两种物质是否存在,设计并进行如下探究活动:
【探究方案设计】
为了确定NaOH的存在,设计了如下方案。
张南同学的方案:取溶液样品少许于试管中,向其中滴加无色酚酞溶液,即可确定溶液中溶质是否含NaOH;
小岗同学的方案:取溶液样品少许于试管中,向其中滴加稀盐酸,即可确定溶液中溶质是否含NaOH;
【交流讨论】
经过小组同学讨论认为小岗同学的方案不可以。
请你表明态度,并对小岗同学的方案进行评价(1)_____________________。由此得出结论,用化学实验的方法验证物质的存在,不仅所加试剂与被检验物质能发生化学反应,还需要(2)________,才能验证物质的存在;经过小组同学讨论后重新设计了整体方案,并进行了如下实验。
【探究实验】
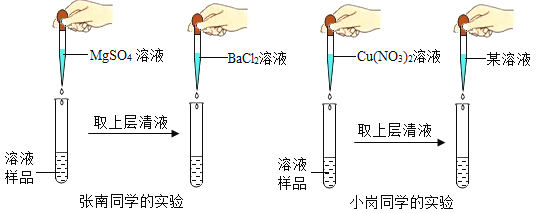
张南同学的实验:重新取溶液样品少许于试管中,向其中滴加足最MgSO4溶液,出现白色沉淀后,取上层清液,再滴加BaCl2溶液,又出现白色沉淀,确定溶液中溶质含NaOH和Na2SO4,请你对张南同学的实验及结论进行评价(3)___________________;小岗同学的实验:重新取溶液样品少许于试管中,其中滴加足量Cu(NO3)2溶液,出现(4) ____________(填实验现象)后,确定溶液中溶质含NaOH,反应的化学方程式为(5)____________;待上述沉淀完全后,取上层清液,再滴加(6) ____________溶液,出现白色沉淀,可确定溶液中溶质含Na2SO4,
【反思与总结】由此得出结论,用化学实验的方法验证同一溶液中两种物质的存在,不仅所加试剂与被检验物质能发生反应,还需要考虑所加试剂(7) ____________,才能验证这两种物质的存在。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活离不开化学,下列说法正确的是
A. 氯化铵和草木灰混合使用,能增强化肥的肥效
B. 二氧化硫和漂白粉混合使用,能增强漂白效果
C. 浓盐酸和高锰酸钾混合使用,能增强高锰酸钾的氧化性
D. 氢氧化钠固体和氧化钙混合使用,能增加吸水能力
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10.0 mL 0.10 mol/L氨水中滴入0.10 mol/L的盐酸,溶液的pH与所加盐酸的体积关系如图所示(假设无气体逸出)。下列有关叙述正确的是( )
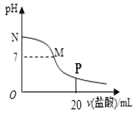
A. M~N间一定存在:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B. M点对应的盐酸体积为10.0mL
C. pH=7的溶液中:c(NH4+)=c(Cl-)=c(H+)=c(OH-)
D. P点处的溶液中存在:2c(NH4+)+2c(NH3·H2O)=c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学反应的自发性叙述中正确的是( )
A.焓变小于0而熵变大于0的反应肯定是自发的
B.焓变和熵变都小于0的反应肯定是自发的
C.焓变和熵变都大于0的反应肯定是自发的
D.熵变小于0而焓变大于0的反应肯定是自发的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. ⅠA族元素的金属性比ⅡA族元素的金属性强
B. ⅣA族元素的氢化物中,稳定性最好的是CH4
C. 同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D. 第3周期元素的离子半径从左到右逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将适量的SO2通入Fe(NO3)3中,溶液逐渐由棕黄色变为浅绿色,但又立即变为棕黄色,继续滴入BaCl2溶液,产生白色沉淀。在上述一系列变化过程中,最终被还原的元素是( )
A.S B.Fe C.Cl D.N
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com