
【题目】常温下PbSO4、PbCO3的溶度积常数分别为1.7×![]() 、7.4×
、7.4×![]() ,下列说法错误的是
,下列说法错误的是
A. PbSO4的饱和溶液中,c(Pb2+)约为1.3×![]()
![]()
B. 反应PbSO4(s)+CO32-(aq) ![]() PbCO3(s)+SO42-(aq)的平衡常数约为4.4×
PbCO3(s)+SO42-(aq)的平衡常数约为4.4×![]()
C. 向c(CO32-)=c(SO42-)的混合液中滴加Pb(NO3)2溶液,先得到PbCO3沉淀
D. PbCO3在水中的溶解度比在Pb(NO3)2溶液中的大
科目:高中化学 来源: 题型:
【题目】M(NO3)2热分解的化学方程式为:2M(NO3)2 ![]() 2MO+4NO2↑+O2↑。加热29.6 g M(NO3)2使其完全分解,在标准状况下收集11200 mL的气体,那么M的摩尔质量是( )
2MO+4NO2↑+O2↑。加热29.6 g M(NO3)2使其完全分解,在标准状况下收集11200 mL的气体,那么M的摩尔质量是( )
A.64 g·mol-1B.24 g·mol-1
C.65 g·mol-1D.40 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:
CO(g)+3H2(g)![]() CH4(g)+H2O(g) H1=-206.2 kJ/mol
CH4(g)+H2O(g) H1=-206.2 kJ/mol
CO(g)+H2O(g)![]() CO2(g)+H2(g) H2
CO2(g)+H2(g) H2
若CO2还原H2生成0.1molCH4(g)和一定量的H2O(g),整个过程中放出的热量为16.5kJ,则△H2=____________。
(2)为研究CO2与CO之间的转化。让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)![]() 2CO(g) H,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示:
2CO(g) H,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示:
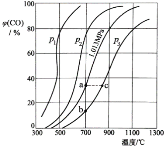
回答下列问题:
①p1、p2、p3的大小关系是______________,图中a、b、c三点对应的平衡常数大小关系是____________。
②900℃、1.013MPa时,1molCO2与足量碳反应达平衡后容器的体积为VL,CO2的转化率为_____________,(保留一位小数)该反应的平衡常数K=_________。
③将②中平衡体系温度降至640℃,压强降至0.1013MPa,重新达到平衡后CO2的体积分数为50%。条件改变时,正反应和逆反应速率如何变化?_______________________________,二者之间有何关系?________________________。

(3)CO2可用于工业制备草酸锌,其原理如图所示(电解液不参加反应),Zn电极是_____极。已知在Pb电极区得到ZnC2O4,则Pb电极上的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,4二氯苯乙酸是生产新型杀虫、杀螨剂螺螨酯的关键中间体,其结构简式如图所示。下列有关说法错误的是( )
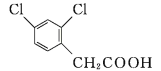
A. 该有机物能发生加成反应、取代反应
B. 该有机物的分子式为C8H6Cl2O2
C. 改变氯原子在苯环上的位置,还可得到8种结构
D. 该有机物分子中所有的碳原子可能同时处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钇钡铜氧(YBa2Cu3O7-x)是一种高温超导材料(其中Y显+3价,Cu显+2、+3价),最早是将BaCO3、Y2(CO3)3和CuCO3混合在高温下反应制备的。
请回答下列问题:
(1)Y(钇)是一种重要的稀土金属,与Sc(钪)同族相邻。则Y原子核外有___________个价电子。Y位于元素周期表的___________区。
(2)在BaCO3中,CO32-的空间构型为___________,C原子采取___________杂化;BaCO3、CaCO3受热分解分别生成BaO、CaO,BaO、CaO熔点较高的是___________ (填化学式)。
(3)基态Cu3+的核外电子排布式为___________。
(4)若YBa2Cu3O7-x(0≤x≤0.5)材料在T ℃下有超导性,当x=0.2时,n(Cu3+)∶n(Cu2+)=___________。
(5)铜有两种氧化物:CuO和Cu2O,后者比前者的热稳定性强,原因是___________。
(6)如图是某种超导材料A的晶胞结构示意图,其化学式为___________。若A的摩尔质量为M g·mol-1,阿伏加德罗常数的值为NA,晶胞参数为apm、apm、bpm,则晶体的密度为___________g·cm-3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物用途广泛。回答下列问题:
(1)在一定条件下,氮气能和水蒸气反应生成氨气和氧气2N2(g)+6H2O(g)=4NH3(g)+3O2(g)△H,与该反应相关的化学键键能数据如下:
化学键 | N≡N | H—O | N—H | O=O |
E(kJ/mol) | 946 | 463 | 391 | 496 |
则该反应的△H=________kJ·mol-1。
(2)在恒容密闭容器中充入2 mol N2O5与1molO2发生反应4NO2 (g) + O2 (g) ![]() 2N2O5 (g) △H。
2N2O5 (g) △H。
①已知在不同温度下测得N2O5的物质的量随时间的变化如图所示,该反应的△H_____0(填“>”“<”或“=”)。高温下该反应能逆向自发进行,其原因是___________________。
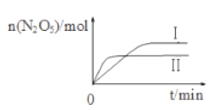
②下列有关该反应的说法正确的是_______(填标号)。
A.扩大容器体积,平衡向逆反应方向移动,混合气体颜色变深
B.恒温恒容,再充入2 mol NO2和1molO2,再次达到平衡时,NO2的转化率增大
C.恒温恒容,当容器内的密度保持不变时,反应达到了平衡状态
D.若该反应的平衡常数增大,则一定是降低了温度
(3)N2O5是一种新型绿色硝化剂,其制备可以用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5,工作原理如图所示。则硼氢化钠燃料电池的负极反应式为_________。

(4)X、Y、Z、W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种。下表是常温下浓度均为0.01molL—1的X、Y、Z、W溶液的pH。将X、Y、Z各1mol同时溶于水中得到混合溶液,则混合溶液中各离子的浓度由大到小的顺序为________。
0.01molL—1的溶液 | X | Y | Z | W |
pH | 12 | 2 | 8.5 | 4.5 |
(5)氮的氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
I:2NO2(g)+NaCl(s) ![]() NaNO3 (s)+ClNO(g) K1
NaNO3 (s)+ClNO(g) K1
Ⅱ:2NO(g)+Cl2 (g) ![]() 2CNO(g) K2
2CNO(g) K2
①4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=____(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=____(用K1、K2表示)。
②在恒温条件下,向2L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10min时反应Ⅱ达到平衡,测得10min内v(ClNO)=7.5×10-3molL-1min-1,则平衡时NO的转化率α1=____;若其他条件不变,反应Ⅱ在恒压条件下进行,平衡时NO的转化率α2__α1(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铜 [Cu2(OH)2CO3]是一种用途广泛的化工原料,实验室以废铜屑为原料制取碱式碳酸铜的步骤如下:
步骤一:废铜屑制硝酸铜
如图,用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液。

步骤二:碱式碳酸铜的制备
向大试管中加入碳酸钠和硝酸铜溶液,水浴加热至70℃左右,用0.4mol/L的NaOH溶液调节pH至8.5,振荡,静置,过滤,用热水洗涤,烘干,得到碱式碳酸铜产品。
完成下列填空:
(1)写出浓硝酸与铜反应的离子方程式___________________________________。
(2)上图装置中NaOH溶液的作用是__________________________________________。
(3)步骤二中,水浴加热所需仪器有_________、________(加热、夹持仪器、石棉网除外);洗涤的目的是______________________________________________。步骤二的滤液中可能含有CO32-,写出检验CO32-的方法_______________________________________。
(4)影响产品产量的主要因素有________________________________________。
(5)若实验得到2.42g样品(只含CuO杂质),取此样品加热至分解完全后,得到1.80g固体,此样品中碱式碳酸铜的质量分数是_________________(保留两位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com