
| A. | 硅酸盐一般不溶于水,它是水泥、陶瓷、玻璃的主要成分 | |
| B. | SiO2与CO2相似,由一个硅原子和两个氧原子构成一个SiO2分子 | |
| C. | SiO2是酸性氧化物,能与水反应生成硅酸 | |
| D. | 硅元素是构成矿物岩石的主要成分之一,其化合态几乎全部是氧化物和硅酸盐 |
分析 A、水泥、玻璃、陶瓷等硅酸盐材料,硅酸钠盐溶于水;
B、二氧化硅不是分子;
C、二氧化硅不溶于水,也不与水反应;
D、硅石及硅酸盐中含有大量硅元素.
解答 解:A、水泥、玻璃、陶瓷等硅酸盐材料,硅酸钠盐溶于水,所以硅酸盐一般不溶于水,它是水泥、陶瓷、玻璃的主要成分,故A正确;
B、二氧化硅不是分子,硅和氧的原子个数比为1:2,故B错误;
C、二氧化硅不溶于水,也不与水反应,故C错误;
D、硅是亲氧元素,在自然界中以化合态存在,是组成硅石和硅酸盐的主要元素,故D正确;
故选AD.
点评 本题考查了硅的性质,知道自然界中硅、Al都属于亲氧元素,导致这两种元素在自然界中不能以游离态存在,题目难度不大.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,将pH=2的盐酸和pH=12的氨水等体积混合:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 0.1mol•L-1 Na2CO3溶液:2c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| C. | 相同温度下,0.6 mol/L氨水溶液与0.3 mol/L氨水溶液中c(OH-)之比是2:1 | |
| D. | 物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中,c(NH4+)的大小关系:①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L | B. | 2mol/L | C. | 3.2mol/L | D. | 4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | w2>2w1 | B. | 2w2=w1 | C. | 2w1=w2 | D. | w1<w2<2w1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
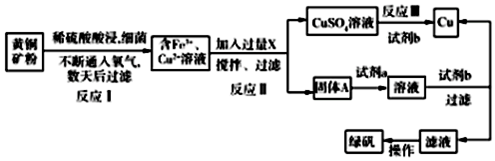
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
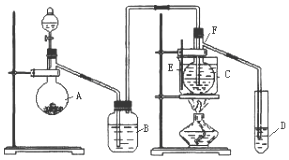
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4个 | B. | 3个 | C. | 2个 | D. | 1个 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 分类标准 | 酸性氧化物 | 非电解质 | |
| 属于该类的物质 | ⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com