
关于化学平衡常数的叙述正确的是( )
A.温度一定,一个化学反应的平衡常数与反应物浓度成正比
B.两种物质反应,不管怎样书写化学方程式,平衡常数不变
C.温度一定时,对于给定的化学反应,正、逆反应的平衡常数互为倒数
D.浓度商Q<K,v正<v逆
科目:高中化学 来源: 题型:
在下列物质中:①CO2 ②NaCl ③MgBr2 ④I2 ⑤NH4Cl ⑥Ca(OH)2 ⑦N2 ⑧H2S ⑨NH3
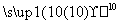 K2O2
K2O2
(1)只有非极性键的是_________________________________;
(2)只有极性键的是___________________________________;
(3)只有离子键的是___________________________________;
(4)有离子键,也有非极性键的是_______________________;
(5)既有离子键,又有极性键的是_______________________;
(6)属于离子化合物的是_______________________________;
(7)属于共价化合物的是_______________________________;
(8)含有配位键的物质是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于原子结构、元素性质的说法正确的是( )
A.非金属元素组成的化合物中只含共价键
B.ⅠA族金属元素是同周期中金属性最强的元素
C.同种元素的原子均有相同的质子数和中子数
D.ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
利用反应2NO(g)+2CO(g)2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )
A.降低温度
B.增大压强同时加催化剂
C.升高温度同时充入N2
D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制硝酸的主要反应是4NH3(g)+5O2(g)4NO(g)+6H2O(g) ΔH=-1025 kJ·mol-1
(1)该反应的平衡常数表达式为K=________;升高温度,K值________(填“增大”或“减小”或“不变”)。
(2)若反应物起始的物质的量相同,下列关系图错误的是______
(填序号)。

(3)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如下表:
| 浓度 时间 | c(NH3) (mol·L-1) | c(O2) (mol·L-1) | c(NO) (mol·L-1) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 1.6 | 0.5 |
①起始时物料比c(O2)c(NH3)>1.25,其原因是________;
②反应在第2min到第4min时,O2的平均反应速率为__________mol·L-1·min-1;
③反应在第2min时改变了反应条件,改变的条件可能是__________(填序号);
a.使用催化剂 b.升高温度
c.充入He气体 d.增加O2的浓度
④反应在第8min时改变的反应条件可能是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应A+B—→C,如果温度每升高10 ℃,反应速率增加为原来的3倍。在10 ℃时,完成反应的20%需要54 min;将温度提高到40 ℃,完成反应的20%需要的时间为( )
A.2 min B.3 min
C.6 min D.9 min
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学反应2AB+D在四种不同的条件下进行,B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表。

据上表,回答下列问题。
(1)在实验1中,反应物A在10~20分钟时间内平均速率为________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=________mol·L-1,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_________________
____________________________________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______(填“>”、“=”或“<”,下同)v1,且c3________1.0 mol·L-1。
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”、“放热”)。理由是___________________________________
_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象预测正确的是 ( )

A.实验I:振荡后静置,上层溶液颜色保持不变
B.实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去
C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色
D.实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1 mol
CuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是( )

A.铜棒为正极,其电极反应式为2H++2e-—→H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过的电子的物质的量为0.2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com