
| A、CaO |
| B、KCl |
| C、MgCl2 |
| D、Na2S |
科目:高中化学 来源: 题型:
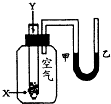 某学生用如右图所示的装置进行化学反应X+2Y→2Z能量变化情况的研究.当往试管中滴加试剂Y时,看到试管中甲处液面下降,乙处液面上升.关于该反应的下列叙述正确的是( )
某学生用如右图所示的装置进行化学反应X+2Y→2Z能量变化情况的研究.当往试管中滴加试剂Y时,看到试管中甲处液面下降,乙处液面上升.关于该反应的下列叙述正确的是( )| A、①②③ | B、①③ | C、②③ | D、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,烧杯中都盛有稀硫酸:
如图所示,烧杯中都盛有稀硫酸:查看答案和解析>>
科目:高中化学 来源: 题型:
2- 4 |
| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 | |||
| B、CH3CH2CHO+H2→CH3CH2CH2OH | |||
C、2CH3CH2OH+O2
| |||
D、2CH3-CH2-OH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分别将Na和Al同时放入冷水中 |
| B、测定等物质的量的Na和Al与酸反应生成H2的体积 |
| C、向Al(OH)3悬浊液中加入足量NaOH溶液 |
| D、用PH计测量NaCl溶液与AlCl3溶液的PH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com