
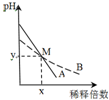
 室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示.下列说法正确的是( )| A. | 稀释前,c(A)>10 c(B) | |
| B. | 中和等浓度等体积的盐酸时,B用的体积较多 | |
| C. | M点时A和B的浓度相等 | |
| D. | 在M点,A、B两种碱溶液中阳离子的物质的量浓度相等 |
分析 A.依据图象分析判断AB稀释相同倍数,A的pH变化大,
B.稀释前A溶液中氢氧根离子浓度大于B溶液中;
C.M点AB溶液pH相同,二者碱性强弱不同;
D.根据电荷守恒分析.
解答 解:A.AB稀释相同倍数,A的pH变化大,则A的碱性强,稀释前,设c(A)=0.1mol/L,c(B)>0.01mol/L,则c(A)<10c(B),故A错误;
B.稀释前A溶液中氢氧根离子浓度大于B溶液中,即A的浓度大于B,所以中和等浓度等体积的盐酸时,A用的体积较多,故B错误;
C.M点AB溶液pH相同,A的碱性强,A的电离度大于B,所以浓度B大于A的浓度,不相等,故C错误;
D.M点AB溶液pH相同,氢氧根离子浓度相同,由电荷守恒c(A+)+c(H+)=c(OH-),c(B+)+c(H+)=c(OH-)可知c(A+)=c(B+),所以M点A、B两种碱溶液中阳离子的物质的量浓度相等,故D正确;
故选D.
点评 本题考查电解质在水中的电离及图象,明确图象中pH的变化及交点的意义是解答本题的关键,题目难度中等,侧重于考查学生的分析能力和读图能力.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液中一定含有Br-、SO42- | |
| B. | 原溶液一定含有Na+,不含Ba2+ | |
| C. | 实验①与上述离子的检验无关,可以省略 | |
| D. | 若要判断原溶液中是否含有Cl-,所需药品有CCl4溶液、Ba(NO3)2溶液和稀HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实际应称Na2CO3质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
| 2.7 | 250mL | 天平、烧杯、玻璃棒、胶头滴管、药匙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚溶液、乙醇、己烯、四氯化碳 | B. | 甲酸、乙酸、乙醛、乙醇 | ||
| C. | 淀粉溶液、乙醇、苯、四氯化碳 | D. | 苯、甲苯、己烯、溴苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com