
 .
.
分析 (1)次外层电子数是最外层电子数$\frac{1}{4}$的元素只能是氖;
(2)1~36号元素,未成对电子数最多的元素外围电子排布为3d54s1,共有6个未成对电子;
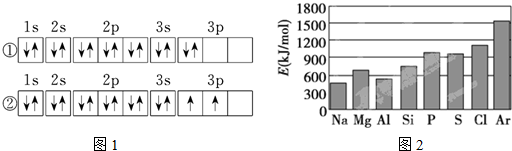
(3)由电子排布图中的电子数知,C元素是硅,根据洪特规则,当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋方向相同;
(4)由图可知,同周期内,随着原子序数的增大,E值变化的总趋势是增大,但原子处于半满、全满是,能量较低,第一电离能高于同周期相邻元素;同主族金属性越强,第一电离能越小.
解答 解:(1)次外层电子数是最外层电子数$\frac{1}{4}$的元素只能是氖,外围电子的电子排布图是 ,故答案为:
,故答案为: ;
;
(2)1~36号元素,未成对电子数最多的元素外围电子排布为3d54s1,共有6个未成对电子,该元素是铬,处于周期表中第四周期第ⅥB族,
故答案为:铬;第四周期第ⅥB族;
(3)由电子排布图中的电子数知,C元素是硅,根据洪特规则,当电子排布在同一能级的不同轨道时,基态原子中的电子总是优先单独占据一个轨道,且自旋方向相同,故硅元素基态原子的电子排布图为②,即另一电子排布图不能作为基态原子的电子排布图是因为它不符合C,
故答案为:②;C;
(4)①由图可知,同周期内,随着原子序数的增大,E值变化的总趋势是增大,故答案为:增大;
②由图可知,同周期内,随着原子序数的增大,E值变化的总趋势是增大,但原子处于半满、全满是,能量较低,第一电离能高于同周期相邻元素,故E氧<E氟,
故答案为:<;
③同主族金属性越强,第一电离能越小则E镁>E钙,故答案为:>.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构推断元素、电子排布规律、第一电离能变化规律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 油脂的水解反应都是皂化反应 | |
| B. | 淀粉水解和纤维素水解得到的最终产物不同 | |
| C. | 蛋白质水解的最终产物均为葡萄糖 | |
| D. | 油脂的水解可得到甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将氢氧化铁溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| C. | 碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2 Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. 的系统命名为3-甲基-戊烷.
的系统命名为3-甲基-戊烷. .
. 中,共平面的碳原子最多有13个,共直线的原子最多有5个,该分子中有4种不同化学环境的H原子.
中,共平面的碳原子最多有13个,共直线的原子最多有5个,该分子中有4种不同化学环境的H原子.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验: .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com