
| A. | 乙醇的沸点高于丙烷 | |
| B. | 油脂和蛋白质都是高分子化合物 | |
| C. | CH2=C(CH3)2的名称是2-甲基-2-丙烯 | |
| D. | 对二甲苯的核磁共振氢谱有4个吸收峰 |
分析 A.醇中含氢键,沸点高;
B.油脂的相对分子质量在10000以下;
C.CH2=C(CH3)2中双键C在1、2号C上;
D.对二甲苯结构对称,苯环上1种H,甲基上1种H.
解答 解:A.醇中含氢键,沸点高,则乙醇的沸点高于丙烷,故A正确;
B.油脂的相对分子质量在10000以下,不是高分子,而蛋白质为高分子,故B错误;
C.CH2=C(CH3)2中双键C在1、2号C上,则CH2=C(CH3)2的名称是2-甲基-1-丙烯,故C错误;
D.对二甲苯结构对称,苯环上1种H,甲基上1种H,则对二甲苯的核磁共振氢谱有2个吸收峰,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的结构、性质、高分子判断及名称等为解答的关键,侧重分析与应用能力的考查,注意有机物的结构,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 含有的中子数为a+b | B. | 含有的电子数为a-n | ||
| C. | 质量数为a+b+n | D. | 1mol该原子的质量约为bg |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
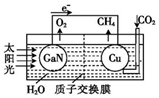 科学家用氮化镓材料与铜组装如图所示人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.下列说法不正确的是( )
科学家用氮化镓材料与铜组装如图所示人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.下列说法不正确的是( )| A. | 该过程是将太阳能转化为化学能的过程 | |
| B. | GaN表面发生氧化反应:2H2O-4 e-═O2↑+4H+ | |
| C. | Cu表面的反应是:CO2+8e-+6H2O═CH4+8OH? | |
| D. | H+透过质子交换膜从左向右迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
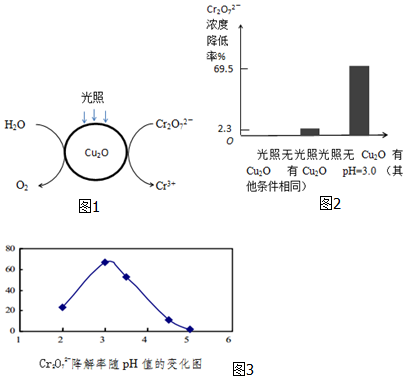
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 皮肤上不慎沾上浓Na OH溶液,立即用稀硫酸冲洗 | |
| B. | 大量氯气泄漏时,应迅速离开现场,并尽快往高处去 | |
| C. | 不慎洒出的酒精在桌上着火时,立即用大量水扑灭 | |
| D. | 金属钠着火时,应立即用沾水的毛巾覆盖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应中Ag和H2S均是还原剂,发生氧化反应 | |
| B. | 银针验毒时,空气中的氧气失去电子 | |
| C. | X的化学式为Ag2S,颜色为黑色,通过观察银针颜色变化来判断死者是否中毒 | |
| D. | 每生成1mo1X,反应转移4mo1 e- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡中加入稀硫酸:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| B. | 将大理石投入到足量盐酸中:CO32-+2H+═CO2↑+H2O | |
| C. | 次氯酸钙溶液中通入少量二氧化碳:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| D. | 硫酸镁溶液和氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2+CaO=CaSiO3 | |
| B. | SiO2+2NaOH=Na2SiO3+H2O | |
| C. | SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO | |
| D. | SiO2+2Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com