
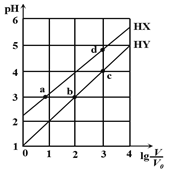
【题目】在浓度均为0.1 mol/L、体积均为V0的HX、HY,分别加水稀释至体积V,pH随lg V/V0的变化关系如右图所示。下列叙述正确的是
A. a、b两点的溶液中:c(X-)>c(Y-)
B. 相同温度下,电离常数K(HX):d>a
C. 溶液中水的的电离程度:d>c>b>a
D. lgV/V0=2时,若同时微热两种液体(不考虑挥发),则c(X-) /c(Y-) 增大
【答案】D
【解析】当lgV/V0=0时,0.1mol/LHY溶液的pH=1,0.1mol/LHX溶液的pH![]() 1,则HY为强酸,HX为弱酸。A项,a点HX溶液中的电荷守恒为c(H+)=c(OH-)+c(X-),b点HY溶液中的电荷守恒为c(H+)=c(OH-)+c(Y-),a点、b点pH相同,两溶液中c(H+)、c(OH-)相等,则a、b两点溶液中c(X-)=c(Y-),错误;B项,稀释时温度不变,电离平衡常数不变,a、d点的K(HX)相等,错误;C项,酸溶液中OH-全部来自水的电离,图中a、b、c、d点的pH由大到小的顺序为:d
1,则HY为强酸,HX为弱酸。A项,a点HX溶液中的电荷守恒为c(H+)=c(OH-)+c(X-),b点HY溶液中的电荷守恒为c(H+)=c(OH-)+c(Y-),a点、b点pH相同,两溶液中c(H+)、c(OH-)相等,则a、b两点溶液中c(X-)=c(Y-),错误;B项,稀释时温度不变,电离平衡常数不变,a、d点的K(HX)相等,错误;C项,酸溶液中OH-全部来自水的电离,图中a、b、c、d点的pH由大到小的顺序为:d![]() c
c![]() a=b,四点溶液中c(OH-)由大到小的顺序为d
a=b,四点溶液中c(OH-)由大到小的顺序为d![]() c
c![]() a=b,溶液中水的电离程度:d
a=b,溶液中水的电离程度:d![]() c
c![]() a=b,错误;D项,当lgV/V0=2时,微热两种溶液,由于HY为强酸,c(Y-)不变,HX为弱酸,升高温度促进HX的电离,c(X-)增大,则c(X-)/c(Y-)增大,正确;答案选D。
a=b,错误;D项,当lgV/V0=2时,微热两种溶液,由于HY为强酸,c(Y-)不变,HX为弱酸,升高温度促进HX的电离,c(X-)增大,则c(X-)/c(Y-)增大,正确;答案选D。


科目:高中化学 来源: 题型:
【题目】标准状况下,a L氢气在过量的bL氯气中燃烧,所得混合物用100mL3.00mol·L-1的NaOH溶液恰好完全吸收,则氯气的体积b为( )
A. 2.24L B. 4.48L C. 3.36L D. 1.12L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.甲同学用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2·xH2O)并测量其结晶水含量。己知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。制取流程如下:

回答下列问题:
(1)溶液A中的金属离子有Fe3+、Fe2+、Cu2+。能检验溶液A中Fe2+的试剂____(填编号)
①KMnO4 ②K3[Fe(CN)6] ③NaOH ④KSCN
(2)试剂①是_____,试剂②是_____。(填化学式)
(3)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x的值,某兴趣小组设计了以下实验方案:称取mg晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再轻为止,冷却,称量所得黑色固体的质量为ng。沉淀洗涤的操作方法是________,根据实验数据测得x=_____(用含m、n的代数式表示)。
II.乙同学设计了一套电解饱和食盐水的实验装置,来验证氯气的某些性质和测定产生的氢气的体积。回答下列问题:

(4)所选仪器接口的连接顺序是A接______,______接______;B接______,______接______;___________请用离子方程式说明淀粉KI溶液变蓝的原因_____________________________。
(5)若装入的饱和食盐水为75mL(氯化钠足量,电解前后溶液体积变化可忽略,假设两极产生的气体全部逸出),当测得氢气为8.4mL(已转换成标准状况下的体积)时停止通电。将U形管内的溶液倒入烧杯,常温时测得溶液的pH约为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铁粉加入100mL稀硫酸中,为中和过量硫酸,且使Fe2+完全转化为Fe(OH)2,共消耗掉2mol·L-1NaOH溶液150mL。原硫酸溶液的浓度是
A. 0.5mol·L-1 B. 1mol·L-1 C. 1.5mol·L-1 D. 2mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质转化关系中,需要加入氧化剂才能实现的是( )
A.Na2O2→O2
B.MnO4﹣→Mn2+
C.Fe2+→Fe3+
D.CO2→HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,X、W同主族; Y、Z同周期;X、Y、Z三种元素形成一种化合物M,25℃时,0.1mol·L-1M的水溶液中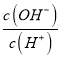 =1.0×10-12。下列说法正确的是
=1.0×10-12。下列说法正确的是
A. 简单离子半径:Y<Z<W
B. X分别与Z、W形成的化合物中,所含化学键类型相同
C. X、Y、Z的非金属性强弱:Y>Z>X
D. Z分别与X、W均可形成具有漂白性的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼镁泥是一种工业废料,主要成份是MgO,还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的工艺流程如下:

已知:NaClO与Mn2+反应产生MnO2沉淀
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀pH | 2.3 | 4.0 | 7.6 | 8.4 |
完全沉淀pH | 4.1 | 5.2 | 9.6 | 10.8 |
根据题意回答下列问题:
(1)请提出两条加快酸解速率的措施__________________。
(2)滤渣的主要成分除MnO2及矿物中其他不溶性杂质外还有_____________ (填化学式),写出生成MnO2的离子方程式_____________ 。
(3)在除去滤渣之前,往往还加一定物质再次调节pH,请选择合适的物质________
A.NaOH B.MgO C.Mg(OH)2 D.氨水
根据表格给出数据写出调节pH的范围___________。
(4)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) | 20 | 50 | 60 | 70 |
MgSO4 | 25.0 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgS4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤___________。再将滤液进行“操作1”,则析出晶体后的溶液(20℃) 中,C(Mg2+)=___________mol/L(该混合溶液的密度为1.2g·cm-3)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不能体现相关主旨的是
A. “水域蓝天,拒绝污染”一严控PM 2.5排放,改善雾霾天气
B. “化学,让生活更美好”一积极开发风力发电,让能源更清洁
C. “节能减排,低碳经济”一综合利用煤和石油,发展绿色化学
D. “化学,引领科技进步”一研究合成光纤技术,让通讯更快捷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成路线如图所示。
![]()
(1)已知AlCl3的熔点为190℃,沸点为178℃,在湖湿的空气中易水解。某实验小组利用下图中装置制备无水AlCl3。
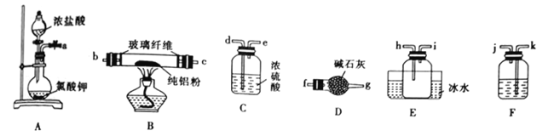
①写出圆底烧瓶中发生反应的离子方程式:_________________。
②按气流方向连接各仪器接口,顺序为a→__________b→c→_______。 (填接口字母)
③装置F中应盛装的试剂是__________,装置D的作用是______________。
(2)AlCl3与NaH反应时,需先将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是______________。
(3)通过测定铝氢化钠与水反应生成氢气的体积来测定铝氢化钠样品的纯度。
①铝氢化的与水反应的化学方程式为______________。
②设计如下四种装置测定铝氢化钠样品的纯度(杂质只有氢化钠)。从简约性、准确性考虑,最恰当的装置是___(填编号)。
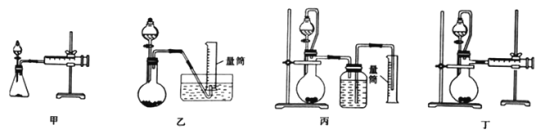
③某同学选用上述最恰当的裴置,称取mg铝氢化钠样品,测得生成气体的体积为VL(已折算为标准状况),重复实验操作三次,测得有关数据如下表所示,则样品中铝氢化钠的纯度为____。
实验次数 | 样品质量m(g) | 气体休积V(L) |
I | 1.20 | 1.907 |
II | 1.20 | 1.904 |
III | 1.20 | 1,901 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com