
利用如图所示装置进行实验,能实现实验目的是(必要时可加热)

选项 | 实验目的 | 甲 | 乙 | 丙 |
A | 制取并收集NH3 | 浓氨水 | CaO | H2O |
B | 制取并验证碳酸酸性比硅酸强 | 浓盐酸 | 大理石 | 硅酸钠溶液 |
C | 制取并验证Cl2没有漂白性 | 浓盐酸 | MnO2 | 干燥的红布条 |
D | 制取并验证SO2具有漂白性 | 70%硫酸 | Na2SO3 | 品红试液 |
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源:2016届福建省莆田市高三上学期期中测试化学试卷(解析版) 题型:选择题
500 mL KNO3和Cu(NO3)2的混合溶液中c(NO)=0.6 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到2.24 L气体(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
A.原混合溶液中c(K+)为0.2 mol·L-1
B.上述电解过程中共转移0.2 mol电子
C.电解得到的Cu的物质的量为0.05 mol
D.电解后溶液中c(H+)为0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016届广西省高三上学期第二次月考化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关。下列说法不正确的是
A.闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺
B.四大发明之一黑火药是由硫黄、硝石、木炭三种物质按一定比例混合制成
C.侯氏制碱法的工艺过程中应用了物质溶解度的差异
D.打磨磁石制作指南针为化学变化
查看答案和解析>>
科目:高中化学 来源:2016届河南省南阳市高三上学期第一次联考化学试卷(解析版) 题型:选择题
下列有关阿伏加德罗常数(NA)的叙述正确的是
A.常温常压下,32克氧气中含有2NA个原子
B.标准状况下,1L己烯完全燃烧后所生成气态产物的分子数为6NA/22.4
C.78g Na2O2晶体中含有的阴离子数目为2NA个
D.1molNa2O2与足量CO2反应转移的电子总数为2NA
查看答案和解析>>
科目:高中化学 来源:2016届山东省淄博市高三上学期第一次月考化学试卷(解析版) 题型:实验题
三氯化磷(PCl3)是一种重要的掺杂剂。实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如下图所示:(部分夹持装置略去)
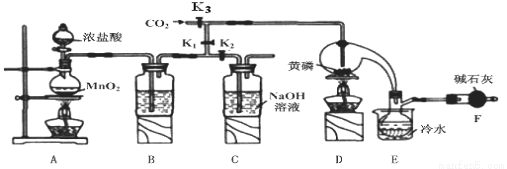
已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5 ;
②PCl3遇水会强烈水解生成 H3PO3和气体;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
物质 | 熔点/℃ | 沸点/℃ |
PCl3 | -112 | 75.5 |
POCl3 | 2 | 105.3 |
请回答下列问题:
(1)B中所装试剂是 ;
E中冷水的作用是 。
(2)F中碱石灰的作用是 。
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷。通干燥CO2的作用是 。
(4)粗产品中常含有POC13、PCl5等。加入黄磷加热除去PCl5后,通过 (填实验操作名称),即可得到较纯净的PCl3。
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为 。
(6)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00 g产品,加水反应后配成250 mL溶液;
②取以上溶液25.00mL,向其中加入10.00 mL 0.1000 mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000 mol/L的Na2S2O3,溶液滴定;
④重复②、③操作,平均消耗0.1000 mol/L Na2S2O3溶液8.40mL。
已知:H3PO3+I2=H3PO4+2HI,I2+2Na2S2O3=2NaI+Na2S4O6,根据上述数据,假设测定过程中没有其他反应,该产品中PCl3的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省淄博市高三上学期第一次月考化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数,下列说法错误的是
A.5.6 g Fe与Br2完全反应,转移电子数为0.3NA
B.常温常压下,3.2 g O3所含的氧原子数为0.2NA
C.1L 0.1mol•L﹣1的NaHCO3溶液中HCO3﹣和CO32﹣离子数之和小于0.1NA
D.常温常压下,22.4 L O2所含的原子数为2NA
查看答案和解析>>
科目:高中化学 来源:2016届四川省广元市高三上学期第二次阶段测理综化学试卷(解析版) 题型:填空题
某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。

(1)X极与电源_________(填“正”或“负”)极相连,氢气从_________(填 “B” 或“C” )口导出。
(2)离子交换膜只允许一类离子通过,则M为__________交换膜(填“阴离子”或“阳离子”,下同),N为_________交换膜。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为_____________________。
(4)若在标准状况下,制得11.2 L氢气,则生成硫酸的质量是_________,转移的电子数为________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省龙海市高一上学期期中测试化学试卷(解析版) 题型:选择题
试管中盛有少量白色固体,可能是铵盐,检验的方法是
A.加NaOH溶液,加热,滴入酚酞试剂
B.加NaOH溶液,加热,滴入紫色石蕊试剂
C.加NaOH溶液,加热,将干燥的红色石蕊试纸靠近试管口
D.加NaOH溶液,加热,将湿润的红色石蕊试纸靠近试管口
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上学期期中测试化学试卷(解析版) 题型:选择题
下列电离方程式错误的是
A.NaHCO3=Na++HCO3- B.NaHSO4=Na++H++SO42-
C.MgCl2=Mg2++2Cl- D.Ba(OH)2=Ba2++2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com