
下列有关NaClO和NaCl混合溶液的叙述正确的是:
A.该溶液中,H+、NH4+、SO42-、Br-可以大量共存
B.该溶液中,Ag+、K+、NO3-、CH3CHO可以大量共存
C.向该溶液中滴入少量FeSO4溶液,反应的离子方程式为:
2Fe2++ClO-+2H+=== Cl-+2Fe3++H2O
D.向该溶液中加入浓盐酸,每产生1molCl2,转移电子约为6.02×1023个
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
四种短周期非金属元素A、B、C、D,原子序数依次增大。A是原子半径最小的元素, B原子的最外层电子数是次外层电子数的两倍,D在地壳中含量最大。请回答:
(1)B元素的原子结构示意图是__________。
(2)化合物CA3的电子式是______________。
(3)BD2与淡黄色固体反应生成D2的反应方程式:_____________________。
(4)丙为含有上述四种元素的常见无机酸式盐,则丙的化学式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CH3—CH===CH2+HBr—→CH3—CHBr—CH3(主要产物)。1 mol某烃A充分燃烧后可以得到8 mol CO2和 4 mol H2O。该烃A在不同条件下能发生如下图所示的一系列变化。

(1)A的化学式:________,A的结构简式:________。
(2)上述反应中,①是________反应,⑦是________反应。(填反应类型)
(3)写出C、D、E、H物质的结构简式:
C____________________,D________________________________________________________________________,
E____________________,H________________________________________________________________________。
(4)写出D—→F反应的化学方程式__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于自然界中氮循环(如右图)的说法不正确的是:
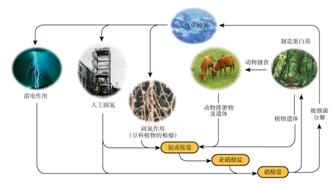
A.但元素均被氧化
B.工业合成氨属于人工固氮
C.含氮无机物和含氮有机物可相互转化
D.碳、氢、氧三种元素也参与了氮循环
查看答案和解析>>
科目:高中化学 来源: 题型:
研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
(1)溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3 -的方程式: 。
-的方程式: 。
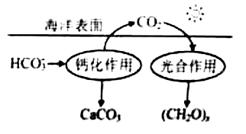
(2)在海洋循环中,通过右图所示的途径固碳。
①写出钙化作用的离子方程式: 。
②同位素示踪法证实光合作用释放出的O2只来自于H2O,用18O标记物质的光合作用的化学方程式如下,将其补充完整: + ===(CH2O)x+x18O2+xH2O
(3)海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
①气提、吸收CO2,用N2从酸化后的还说中吹出CO2并用碱液吸收(装置示意图如下),将虚线框中的装置补充完整并标出所用试剂。
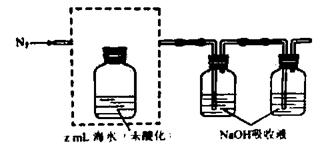
②滴定。将吸收液洗后的无机碳转化为NaHCO3,再用xmol/LHCl溶液滴定,消耗ymlHCl溶液,海水中溶解无机碳的浓度=  mol/L。
mol/L。
(4)利用右图所示装置从海水中提取CO2,有利于减少环境温室气体含量。
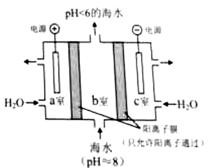
①结合方程式简述提取CO2的原理: 。
②用该装置产生的物质处理b室排出的海水,合格后排回大海。处理至合格的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
四苯基乙烯(TFE)及其衍生物具有诱导发光特性,在 光电材料等领域应用前景广泛。以下是TFE的两条合成路线(部分试剂及反应条件省略):
光电材料等领域应用前景广泛。以下是TFE的两条合成路线(部分试剂及反应条件省略):
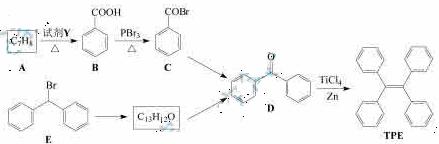
(1)A的名称是______;试剂Y为_____。
(2)B →C的反应类型为_______;B中官能团的名称是______,D中官能团的名称是______.。
→C的反应类型为_______;B中官能团的名称是______,D中官能团的名称是______.。
(3)E→F的化学方程式是_______________________。
(4)W是D的同分异构体,具有下列结构特征:①属于萘(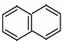 )的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:_____。
)的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:_____。
(5)下列叙述正确的是______。
a.B的酸性比苯酚强 b.D不能发生还原反应
c.E含有3种不同化学环境的氢 d.TPE既属于芳香烃也属于烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,将0.05 mol Na2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质。有关结论正确的是
| 加入的物质 | 结论 | |
| A | 50mL 1 mol·L-1H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
| B | 0.05molCaO | 溶液中 |
| C | 50mL H2O | 由水电离出的c(H+)·c(OH—)不变 |
| D | 0.1molNaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学---物质结构与性质]
氟在自然界中常以CaF2的形式存在。
(1)下列关于CaF2的表述正确的是_______。
a.Ca2+与F-间仅存在静电吸引作用
b.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
c.阴阳离子比为2:1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是________(用离子方程式表示)。
已知AlF63-在溶液中可稳定存在。
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为______________,其中氧原子的杂化方式为_________。
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) △H=-313kJ·mol-1,F-F键的键能为159kJ·mol-1,Cl-Cl键的键能为242kJ·mol-1,则ClF3中Cl-F键的平均键能为______kJ·mol-1。ClF3的熔、沸点比BrF3的________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化锰在生产、生活中有广泛应用。
(1)锌—锰碱性电池广泛应用于日常生活。电池的总反应式为
Zn(s)+2MnO2(s)+2H2O(l)===Zn(OH)2(s)+2MnOOH(s)。
该电池的正极反应式为 。
(2)某学习小组拟以废旧干电池为原料制取锰,简易流程如下:
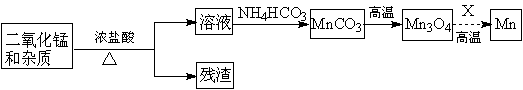
①加入浓盐酸溶于废旧电池内黑色物质过程中保持通风,其原因是 。
②从产品纯度、环保等角度考虑,X宜选择 (填代号)。
A.焦炭 B.铝 C.氢气 D.一氧化碳
③写出碳酸锰在空气中灼烧生成四氧化三锰的化学方程式 。
(3)电解硫酸锰溶液法制锰又叫湿法冶锰。以菱锰矿(主要成份是MnCO3,主要杂质是Fe2+、Co2+、Ni2+)为原料制备锰的工艺流程如下:
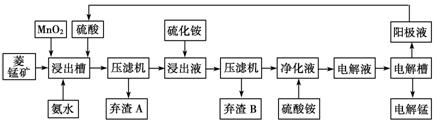
已知:NiS 、CoS均难溶于水。部分氢氧化物的pH如下表:(若某离子浓度小于等于105mol·L1,则认为完全沉淀)
| 物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 | 2.7 |
| 完全沉淀pH | 9.7 | 8.4 | 8.2 | 9.8 | 3.8 |
①用离子方程式表示加入二氧化锰的作用 。
②加入氨水调节浸出槽中溶液的pH范围: 。
③弃渣B可能含有的物质为 。
④电解槽阴极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com