
| A. | 200mL 1mol/L的NaCl溶液 | B. | 150 mL 1mol/L的MgCl2溶液 | ||
| C. | 100mL 1mol/L的HCl溶液 | D. | 50mL 1mol/L的AlCl3溶液 |
分析 根据物质的化学式及物质的物质的量浓度来计算氯离子的物质的量浓度,离子的浓度取决于电解质的物质的量浓度及电解质中含有氯离子的数目,而与体积无关系.
解答 解:A、200mL 1mol/L的NaCl溶液中,Cl-浓度为:1mol/L×1=1mol/L;
B、150mL 1mol/L的MgCl2溶液中,Cl-浓度为:1mol/L×2=2mol/L;
C、100mL 1mol/L的HCl溶液中,Cl-浓度为:1mol/L×1=1mol/L;
D、50mL 1mol/L的AlCl3溶液中,Cl-浓度为:1mol/L×3=3mol/L;
所以氯离子浓度最大的是D,
故选D.
点评 本题考查一定物质的量浓度溶液中所含微粒的物质的量浓度,题目难度中等,注意明确所含微粒的物质的量浓度与所取溶液的体积大小无关.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{29}^{64}$Cu 的核电荷数为 29 | B. | ${\;}_{29}^{64}$Cu 的质子数为 35 | ||
| C. | ${\;}_{29}^{64}$Cu 的中子数为 64 | D. | ${\;}_{29}^{64}$的核外电子数为 64 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>R>Z | |
| B. | W的气态氢化物的热稳定性比Y的强 | |
| C. | Z与W形成的是离子化合物 | |
| D. | W的最高价氧化物对应水化物酸性比R的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 混合气体中一定有甲烷 | B. | 混合气体中一定有甲烷和乙烯 | ||
| C. | 混合气体中一定有乙炔 | D. | 混合气体中一定没有乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | VA=3.0mol•L-1•min-1 | B. | VB=0.2mol•L-1•s-1 | ||
| C. | VC=4.8mol•L-1•min-1 | D. | VD=4.0mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
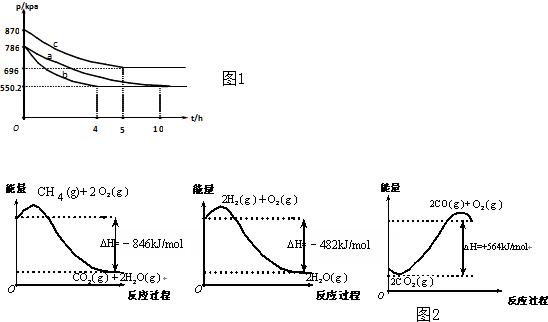
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
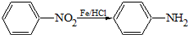 (苯胺,易被氧化).甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物.以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下.
(苯胺,易被氧化).甲苯是一种重要的有机化工原料,可用来合成多种重要的有机物.以甲苯为初始原料合成阿司匹林等有机物的转化关系图(部分产物、合成路线、反应条件略去)如下.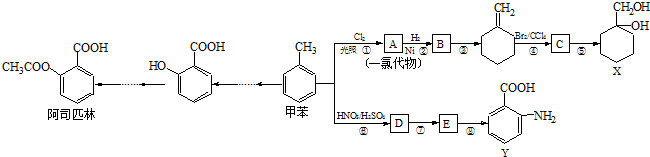
 ,C
,C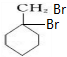 ,E
,E .
.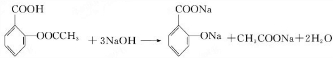 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、AlO2-、CrO42-、CO32- | B. | Na+、AlO2-、CO32- | ||
| C. | Na+、AlO2-、CO32-、SO42- | D. | Na+、Ba2+、AlO2-、CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com