
【题目】尿素[CO(NH2)2] 是一种重要的氮肥,在工农业生产中广泛应用。
(1)工业制备尿素的反应2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(g)。温度为TK时,将68gNH3和88gCO2充入容积为100L的恒容密闭容器中,发生上述反应。测得平衡时CO2和H2O(g)物质的量相等。下列叙述正确的是____________。
CO(NH2)2(l)+H2O(g)。温度为TK时,将68gNH3和88gCO2充入容积为100L的恒容密闭容器中,发生上述反应。测得平衡时CO2和H2O(g)物质的量相等。下列叙述正确的是____________。
a.平衡时,NH3的浓度为0.02 molL1
b.当v(NH3)正=2v(H2O)逆时,反应达到平衡状态
c.若在恒温恒压条件下充入稀有气体,平衡发生正向移动
d.加入适当的催化剂可提高CO2的转化率
(2)尿素溶于水缓慢水解产生碳酸铵,碳酸铵溶液显碱性,原因是___________;碳酸铵溶液中离子浓度由大到小的顺序为_____________;如果将一定浓度的碳酸铵溶液加入到相同浓度的稀BaCl2和ZnCl2混合液中,首先析出的沉淀是__________。(已知Ksp(BaCO3)=5.1×10-9mol2L-2,Ksp(ZnCO3)=1.4×10-11 mol2L-2)
(3)用甲醛法可以间接测定尿素含氮量。尿素通过处理转化为铵盐,甲醛与NH4+作用,其反应如下:4NH4++6HCHO=(CH2)6N4H++3H++6H2O。所生成的H+和(CH2)6N4H+都可与NaOH溶液反应,用NaOH标准溶液滴定时采用酚酞作指示剂。
称取Wg尿素样品,经转化后得到1000mL溶液,量取25.00mL放入锥形瓶中,滴加2滴酚酞,用0.1000molL-1NaOH标准溶液滴定,滴定至终点时,消耗碱液体积20.50mL。
① 滴定至终点的现象是__________________________。
② 该尿素样品的纯度为__________________________。
【答案】ab 碳酸根离子水解(显碱性)程度大于铵根离子水解(显酸性) c(NH4+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) ZnCO3 当滴加最后一滴NaOH溶液,锥形瓶中液体出现浅红色,半分钟内不褪去(不立即褪去) 2.46/W×100%
【解析】
利用三段式计算平衡组成、判断平衡状态及分析外因对化学平衡的影响;根据溶液的酸碱性判断水解程度的大小并比较离子浓度,根据Ksp数据分析沉淀的先后;运用中和滴定原理分析滴定终点现象,并由关系式计算样品纯度。
(1)68gNH3、88gCO2的物质的量分别是4mol、2mol,设转化的CO2物质的量为x。
T K、100L 2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(g)
CO(NH2)2(l)+H2O(g)
起始/mol: 4 2 0 0
转化/mol: 2x x x x
平衡/mol: 4-2x 2-x x x
因平衡时CO2和H2O(g)物质的量相等,即2-x=x,得x=1。
a.平衡时,NH3的浓度为(4-2x)mol÷100L=0.02 molL1;
b.v(NH3)正=2v(H2O)逆,即不同物质表示的正逆反应速率之比等于化学计量数之比,反应达到平衡状态;
c.在恒温恒压条件下充入稀有气体,相当于减小平衡体系的压强,使平衡逆向移动;
d.催化剂不能使化学平衡发生移动,不能提高CO2的转化率。
正确的是ab。
(2)碳酸铵溶于水完全电离①:(NH4)2CO3=2NH4++CO32-,NH4+水解②:NH4++H2O![]() NH3·H2O+H+,CO32-以第一步水解为主③:CO32-+H2O
NH3·H2O+H+,CO32-以第一步水解为主③:CO32-+H2O![]() HCO3-+OH-。碳酸根离子水解程度大于铵根离子水解程度,使溶液呈碱性。据①得c(NH4+)>c(CO32-),据③和水电离得c(OH-)>c(HCO3-),由溶液呈碱性知c(H+)最小,故c(NH4+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。浓度相同的稀BaCl2和ZnCl2混合液中加入碳酸铵溶液时,因Ksp(ZnCO3)<Ksp(BaCO3),故先析出ZnCO3沉淀。
HCO3-+OH-。碳酸根离子水解程度大于铵根离子水解程度,使溶液呈碱性。据①得c(NH4+)>c(CO32-),据③和水电离得c(OH-)>c(HCO3-),由溶液呈碱性知c(H+)最小,故c(NH4+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。浓度相同的稀BaCl2和ZnCl2混合液中加入碳酸铵溶液时,因Ksp(ZnCO3)<Ksp(BaCO3),故先析出ZnCO3沉淀。
(3)尿素转化为铵盐、与甲醛作用后溶液呈酸性,滴入酚酞后溶液无色。随着NaOH标准溶液的加入,溶液的pH增大,当滴加最后一滴NaOH溶液,锥形瓶中液体出现浅红色,且半分钟内不褪去(不立即褪去),即为滴定终点。
据2CO(NH2)2~2(NH4)2CO3~(CH2)6N4H++3H+~4NaOH
n[CO(NH2)2]=![]() n(NaOH)=
n(NaOH)=![]() ×0.1000molL-1×20.50×10-3L=1.025×10-3mol,
×0.1000molL-1×20.50×10-3L=1.025×10-3mol,
尿素样品的纯度=![]() ×100%=
×100%=![]() ×100%。
×100%。


科目:高中化学 来源: 题型:
【题目】下列关于苯的同系物的说法错误的是
A.对苯的同系物命名时必须以苯作为母体,其他的基团作为取代基
B.二甲苯可以以邻、间、对这种习惯命名法进行命名
C.二甲苯也可以用系统命名法进行命名
D.分子式是C8H10的苯的同系物有4种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A. 用过滤法无法除去Fe(OH)3胶体中的FeCl3
B. FeCl3、Na2O2、Cu2S均可由相应单质直接化合生成
C. 从分类的角度看,混合物、分散系、胶体的从属关系如图所示:
![]()
D. 硫酸厂附近的雨水样品在空气中放置2小时后,测得pH变小,因为样品吸收了空气中的CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应:2SO2(g)+O2(g)![]() 2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
2SO3(g),下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
A. 增大压强 B. 升高温度 C. 使用催化剂 D. 多充O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用黄铜矿(CuFeS2)冶炼铜,同时还可得到多种物质。工业冶炼铜的化学方程式是:8CuFeS2+21O2![]() 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
(1)CuFeS2中Fe的化合价为+2,反应中被还原的元素是氧元素和____________。
(2)用少量黄铜矿冶炼铜产生的炉渣(主要含Fe2O3、FeO、SiO2、Al2O3)模拟制铁红(Fe2O3),进行如下实验。
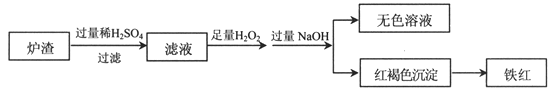
①滤液中的阳离子有Fe3+、Fe2+、H+、_____________。
②为确认滤液中含Fe2+,下列实验方案和预期现象正确的是____(填序号)。
实验方案 | 预期现象 | |
a | 加NaOH溶液 | 产生白色沉淀,变灰绿再变红褐 |
b | 先加KSCN溶液,再加氯水 | 先无明显现象,后变红 |
c | 加酸性KMnO4溶液 | 紫色褪去 |
d | 先加氯水,再加KSCN溶液 | 溶液先变黄,再变红 |
③滤液在酸性条件下,与H2O2反应的离子方程式是_________________________。
(3)m克铝热剂(氧化铁与铝)恰好完全反应,则该反应中氧化产物与还原产物的质量比是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是
A. 1/2N2(g)+H2O(g ) ===1/2N2H4(g)+1/2O2(g) ΔH=+267 kJ·mol-1
B. N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-133.5 kJ·mol-1
C. N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=+534 kJ·mol-1
D. N2H4(g)+O2(g)===N2(g)+2H2O(l) ΔH=-534 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向盛有氯化钡稀溶液的甲、乙两试管中分别通入SO2至饱和,若继续向甲试管中加入足量H2O2溶液,向乙试管中加入足量氢氧化钾溶液,则下列叙述正确的是( )
A.甲、乙两试管中都有白色沉淀生成
B.甲、乙两试管中都没有白色沉淀生成
C.甲试管中没有白色沉淀生成而乙试管中有
D.甲试管中有白色沉淀生成而乙试管中没有
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金、铁合金、硅酸盐都是广泛的建筑材料。回答下列问题
(1)铝的原子结构示意图为___________;在周期表中第___周期,第____族;铝是一种活泼的金属,但在空气中不易被腐蚀,原因是________________________________(用化学方程式表示);写出铝与烧碱反应的离子方程式___________________。
(2)钢是用途最广、用量最多的铁合金,某种钢由铁和另一种元素组成,将少量的钢样品与足量热的浓硫酸充分反应生成两种气体,写出生成两种气体的化学方程式________________________;用长滴管向硫酸亚铁溶液中滴加煮沸过的氢氧化钠溶液,观察到的现象是______________;反应的化学方程式为_________________________;______________。
(3)滑石粉的主要成分是Mg3[Si4O10](OH)2,用氧化物表示其组成:______;二氧化硅能与一种酸反应,可根据此反应原理制雕花玻璃,这种酸是_______;常用的硅酸盐产品有_____、 _______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是

A.该反应的焓变△H>0
B.图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com