
��֪W��X��Y��ZΪ������Ԫ�أ�W��Zͬ���壬X��Y��Zͬ���ڣ�W����̬�⻯����ȶ��Դ���Z����̬�⻯����ȶ��ԣ�X��YΪ����Ԫ�أ�X�������ӵ�������С��Y�������ӵ������ԡ�����˵����ȷ����(����)
A��X��Y��Z��W��ԭ�Ӱ뾶���μ�С
B��W��X�γɵĻ�������ֻ�����Ӽ�
C��W����̬�⻯��ķе�һ������Z����̬�⻯��ķе�
D����W��Y��ԭ���������5��������γɻ�����Ļ�ѧʽһ��ΪY2W3
 ������ϵ�д�
������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2�������Ϊԭ����ȡ1��2������������Ҫ�����ķ�ӦΪ �� ��
A.�ӳɡ���ȥ��ȡ�� B.��ȥ���ӳɡ�ȡ��
C.��ȥ��ȡ�����ӳ� D.ȡ������ȥ���ӳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�л���Ľṹ���á�����ʽ����ʾ����CH3��CH===CH��CH3�ɼ�дΪ ���л���X�ļ���ʽΪ
���л���X�ļ���ʽΪ ������˵������ȷ����
������˵������ȷ����
A��X�Ļ�ѧʽΪC8H8
B���л���Y��X��ͬ���칹�壬�����ڷ���������Y�Ľṹ��ʽΪ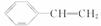
C��X��ʹ���Եĸ��������Һ��ɫ
D��X��������H2��һ�������·�Ӧ�����ɻ�״�ı�����Z��Z��һ�ȴ�����4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
25��ʱ����֪����ĵ��볣����K(CH3COOH) = 1.8 ��10��5��K1(H2CO3) = 4.4 ��10��7��K2(H2CO3) = 4.7 �� 10��11��K(HClO) = 4.0 ��10��8��������˵����ȷ����
A��������ˮ��̼�����Ʋ���Ӧ
B��25��ʱ��0.1mol/L�Ĵ�����Һ��0.01mol/L�Ĵ�����Һ�У�Kaǰ��С�ں���
C��NaClO��Һ��ͨ������������̼�ķ�ӦΪ��2NaClO+CO2+ H2O = Na2CO3 +2HClO
D�������ʵ���Ũ�ȵ�̼������Һ����������Һ������������Һ��pH
pH(Na2CO3)��pH(NaClO)��pH(CH3COONa)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ʵĽṹ�������ʣ����ʷ�ӳ��ṹ�ص㡣
��1�����ʯ��ʯī��̼Ԫ�ص����ֳ������ʣ�������������ȷ����
a�����ʯ��̼ԭ�ӵ��ӻ�����Ϊsp3�ӻ���ʯī��̼ԭ�ӵ��ӻ�����Ϊsp2�ӻ���
b�������й��ۼ��ļ��������ʯ��C��C<ʯī��C��C;
c��������۵㣺���ʯ< ʯī
d�������й��ۼ��ļ��ǣ����ʯ>ʯī
 ��2��ijʯ��ķ��ӽṹ����ͼ��ʾ��
��2��ijʯ��ķ��ӽṹ����ͼ��ʾ��
��ʯ���������Ԫ���У���̬ԭ��2p����������ɵ����ӵ��� ����Ԫ�ط��ţ��� ����������Ԫ���γɵ��������͵�һ���������� ���ѧʽ����
�ڸ�ʯ�����ܽ���ˮ���������ܵ�ԭ���� ��
��3��ͭ����Ͻ�����������ʹ�õĽ������ϡ�
��NF3����NH3��F2��Cu���������·�Ӧֱ�ӵõ���4NH3��3F2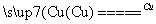 NF3��3NH4F
NF3��3NH4F
 ������ѧ����ʽ�е�5�����������ľ���������_______(�����)��
������ѧ����ʽ�е�5�����������ľ���������_______(�����)��
a�����Ӿ��� b�����Ӿ��� c��ԭ�Ӿ��� d����������
�ڽ���ͭ��ȡ��ͼ��ʾ�ѻ���ʽ���ɳ�Ϊ_____�ѻ�����Cu������
Cuԭ�ӵ���λ��Ϊ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Ԫ��X��Y��Z��W��ԭ��������������X���γɻ���������Ԫ����X�������ϼ�Ϊ��1�ͣ�1��Yԭ�������������Ǵ�����3����Z��X����ͬһ���壬W��ԭ��������Y��2����������������ȷ����(����)
A��ԭ�Ӱ뾶�Ĵ�С˳��rZ>rW>rY>rX
B��Ԫ��Y�ļ���̬�⻯������ȶ��Ա�W����
C��������Z2Y2��X2Y��Ӧʱ��Z2Y2�������������ǻ�ԭ��
D����X��Y��Z��W����Ԫ����ɵĻ�������ˮ��Һһ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�ܱ������з�����Ӧ��2X(g)��Y(g)aZ(g)����H��Q kJ��mol��1����ʼ�������2��1��X��Y���뷴Ӧ���У�һ�������·�����Ӧ��ͼ��ͼ���Ǹ��ݷ�Ӧ���Ƶ�ͼ�������й�˵����ȷ����(����)
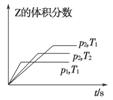
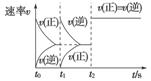
�ס�������������������
A��ͼ�ף�p1>p2��a<3
B��ͼ�ף�T1<T2��Q>0
C��ͼ�ң�t1ʱ��ʾ���¡���ѹ�����£���ƽ����ϵ�г���һ������Z����
D��ͼ�ң����a��3��t2ʱ��ʾ����ϵ�м����˴���������ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B��C����ѧ�������ֵ��ʣ�A��B��C������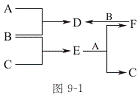 ����֮��ķ�Ӧ��ϵ��ͼ91��ʾ������B��D��E��F��ˮ��Һ�����ԡ���D��C��E��F�ҳ�����ֻ��BΪ��̬����A��B��C�ֱ�Ϊ(����)
����֮��ķ�Ӧ��ϵ��ͼ91��ʾ������B��D��E��F��ˮ��Һ�����ԡ���D��C��E��F�ҳ�����ֻ��BΪ��̬����A��B��C�ֱ�Ϊ(����)
A��Fe��Cl2��Cu B��Fe��Cl2��H2
C��Cu��Cl2��Fe D��Fe��Cl2��Mg
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ʾΪ���ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼۣ����ݱ�����Ϣ�ж�����������ȷ����(����)
| Ԫ�ش��� | A | B | C | D | E |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| ��Ҫ���ϼ� | ��2 | ��3 | ��6����2 | ��1 | ��1 |
A.A��B�����Ӱ뾶��С��ϵΪB3��>A2��
B��D��E�γɵļ����ӵĻ�ԭ�ԣ�E��>D��
C����̬�⻯����ȶ��ԣ�HD<H2C
D������������Ӧ��ˮ��������ԣ�H2CO4>HEO4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com