
| 实验步骤 | 预期现象与结论 |
| 步骤1: | 部分固体不溶解 |
| 步骤2: | |
| 步骤3:继续步骤2中的(2),进行固液分离,用蒸馏水洗涤固体至洗涤液无色.取少量固体于试管中,滴加过量HCl后,静置,取上层清液,滴加适量H2O2,充分振荡后滴加KSCN. |
分析 (1)K离子的检验采用焰色反应来检验,透过蓝色钴玻璃,观察到紫色的火焰;
(2)①根据题意:固体产物中,铁元素不可能以三价形式存在来提出合理假设,可能为+2价或0价;
②金属铁可以和硫酸铜发生置换反应,但是氧化亚铁不可以,根据二者性质的区别知识来回答.
解答 解:(1)可以验证钾离子来确定是否存在碳酸钾,钾离子的检验可以用焰色反应检验,透过蓝色钴玻璃,观察到紫色的火焰,
故答案为:利用焰色反应,透过蓝色钴玻璃,观察到紫色的火焰;
(2)①根据题意:固体产物中,铁元素不可能以三价形式存在,所以存在的可能是0价或是+2价的铁元素的单质或是化合物,
故答案为:全部为FeO,同时存在铁单质和FeO;
③金属铁不溶于水中,但是可以和硫酸铜发生置换反应,生成金属铜和硫酸亚铁,氧化亚铁不溶于水,可以和盐酸反应生成氯化冶铁和水,可以检验亚铁离子的存在进而确定氧化亚铁的存在,
故答案为:
| 实验步骤 | 预期现象与结论 |
| 步骤1:取适量固体产物与试管中,加入足量蒸馏水,充分振荡使碳酸钾完全溶解.分离不溶固体与溶液,用蒸馏水充分洗涤不溶固体 | |
| 步骤2:向试管中加入适量硫酸铜溶液,再加入少量不溶固体,充分振荡 | (1)若蓝色溶液颜色及加入的不溶固体无明显变化,则假设2成立. (2)若蓝色溶液颜色明显改变,且有暗红色固体生成,则证明有铁单质存在 |
| 结合步骤2中的(2): (1)若溶液基本无色,则假设1成立 (2)若溶液呈血红色,则假设3成立 |
点评 本题目考查考生对元素及其化合物性质的掌握,对物质进行检验的实验技能,考查考生运用相关知识对实验提出假设及设计方案的能力,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们互为同位素 | B. | 原子核中的中子数相同 | ||
| C. | 具有相同的质子数 | D. | 23595Am比23592U少3个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
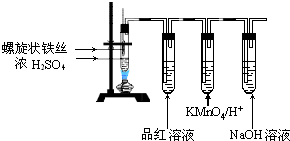
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
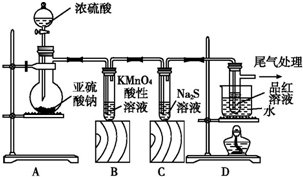
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L NH3中含氮原子数为 NA | |
| B. | 1 mol Na2O2与水完全反应时转移的电子数为NA | |
| C. | 100 mL 2.0 mol•L-1 NH4HCO3溶液中NH4+数为0.2NA | |
| D. | 1 mol O2和2 mol SO2在密闭容器中充分反应后的分子数等于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
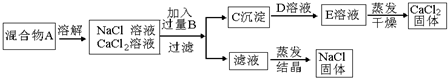
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
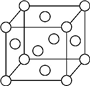 A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com