
| A�� | �٢ڢ� | B�� | �ڢ� | C�� | �ۢܢ� | D�� | �ڢ� |
���� �ٱ�״��ˮ�������壻
������n=$\frac{m}{M}$�������ʵ�������ȼ�����ɹ������Ƽ������ת�ƣ�
��������Ǽ����Ӻ���������ӹ��ɣ�
������n=$\frac{m}{M}$�������ʵ��������O2-���ӽṹ�����������
����CO2��O2��ɵĻ��������ж�����2����ԭ�ӣ�NA���������ʵ���Ϊ1mol��
��� �⣺�ٱ�״��ˮ�������壬�ʢٴ���
������n=$\frac{m}{M}$�������ʵ���=$\frac{23g}{23g/mol}$=1mol����ȼ�����ɹ������Ƽ������ת��NA���ʢ���ȷ��
��������Ǽ����Ӻ���������ӹ��ɣ�1mol ����������������������Ϊ2NA���ʢ۴���
������n=$\frac{m}{M}$�������ʵ���=$\frac{32g}{32g/mol}$=1mol�����O2-���ӽṹ���������17NA���ʢܴ���
����CO2��O2��ɵĻ��������ж�����2����ԭ�ӣ�NA���������ʵ���Ϊ1mol����CO2��O2��ɵĻ�����й��и�NA���ӣ����е���ԭ����Ϊ2NA���ʢ���ȷ��
��ѡB��
���� ���⿼���˰���٤�������ķ���Ӧ�ã���Ҫ�����ʽṹ�������������жϣ�����Ħ�����������Ӧ�ã����ջ����ǹؼ�����Ŀ�ϼ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
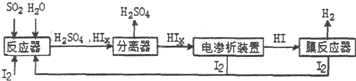
��
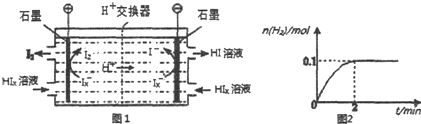
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
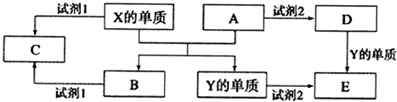
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ˮ�м��������ƾ������Խ��ⵥ����ȡ���� | |
| B�� | ����ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ֧�ܿ� | |
| C�� | ��Һʱ����Һ©���²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� | |
| D�� | ����ʱ������Һ�г��ִ�������ʱ��ֹͣ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ѡ�� | ���� | ������ | ���������������ӷ�Ӧ����ʽ |
| A | pH=1����Һ | Fe2+��Al3+��Cl-��MnO4- | 10Cl-+2MnO4-+16H+�T2Mn2++5Cl2��+8H2O |
| B | ��������Ӧ������������Һ | K+��NO3-��Cl-��NH4+ | NH4++OH-�TNH3•H2O |
| C | ������c��H+��/c��OH��-=10-10����Һ | Na+��Cl-��S2-��SO32- | SO32-+2S2-+6H+�T3S��+3H2O |
| D | ���д���H+������Һ | Na+��Cu2+��AlO2-��SiO32- | 2H++SiO32-�TH2SiO3�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
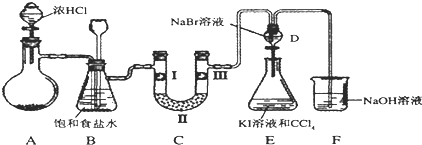
| a | b | c | d | |
| I | �������ɫ���� | �������ɫ���� | ʪ�����ɫ���� | ʪ�����ɫ���� |
| II | ��ʯ�� | ��ˮ�Ȼ��� | ��ʯ�� | ��ˮ�Ȼ��� |
| III | ʪ�����ɫ���� | ʪ�����ɫ���� | �������ɫ���� | �������ɫ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com