
已知热化学方程式:
H2O(g)=H2(g) + 1/2O2(g) △H = +241.8kJ/mol
H2(g)+ 1/2O2(g) = H2O(1) △H = -285.8kJ/mol
当1g液态水变为水蒸气时,其热量变化是( )
A.吸热88kJ B. 吸热2.44KJ C.放热44kJ D. 吸热44KJ
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
B.78 g苯含有C===C键的数目为3 NA
C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,将a mol/L的氨水与b mol/L盐酸等体积混合,下列有关推论不正确的是( )
A.若混合后溶液pH=7,则c(NH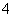 )=c(Cl-)
)=c(Cl-)
B.若b=2a,则c(Cl-)>c(NH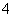 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
C.若a=2b,则c(NH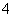 )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
D.若混合后溶液满足c(H+)=c(OH-)+c(NH3·H2O),则可推出a=b
查看答案和解析>>
科目:高中化学 来源: 题型:
碱式碳酸铝镁
[ MgaAlb(OH)c(CO3)d·xH2O]常用作塑料阻燃剂。
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和____________。
(2)MgaAlb(OH)c(CO3)d·xH2O中a、b、c、d的代数关系式为________。
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390 g样品与足量稀盐酸充分反应,生成CO2 0.560 L(已换算成标准状况下)。
②另取一定量样品在空气中加热,样品的固体残留率(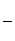 ×100%)随温度的变化如图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
×100%)随温度的变化如图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。
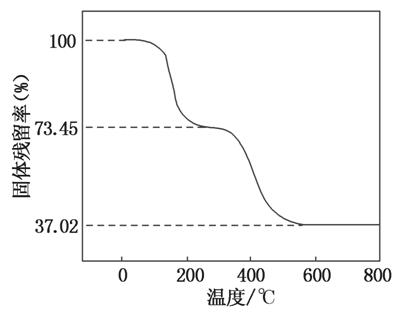
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)n(CO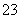 )(写出计算过程)。
)(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有A、B、C、D、E五种短周期主族元素,其原子序数依次增大,它们之间关系如下:
Ⅰ.原子半径:A < C < B < E<D
Ⅱ.原子的核外电子层数:B = C = 2A
Ⅲ.B元素的主要化合价:最高正价 +最低负价 = 2
Ⅳ.C是周期表中非金属性最强的元素
V.原子的最外层电子数:B + D = 8
VI.E是同周期中半径最小的原子
请回答:
(1)实验室制取E的单质反应离子方程式为_____________________________________。
(2)只有A和B两种元素组成的属于离子晶体的化合物可能为 (用化学式表示)。
(3)由D元素形成的氢氧化物,与强碱溶液反应的离子方程式为 。
下列可作为比较D和Mg金属性强弱的方法是_______(填代号)。
a.测两种元素单质的硬度和熔、沸点 b. 比较最高价氧化物对应的水化物的碱性强弱
c.比较单质与同浓度盐酸反应的剧烈程度 d.. 比较两种元素在化合物中化合价的高低
(4)由B、C元素组成的化合物BC3,该化合物具有强氧化性,与水反应生成两种酸和一种无色气体,该气体常温下遇空气变红棕色,写出该化合物与水反应的化学方程式 ______________________ ______________ ________ 。
(5)由A、B和C三种元素组成的盐,常温下其水溶液显酸性,写出检验该盐中所含阳离子的离子方程式 ;
 (6)下图Ⅰ、Ⅱ分别是甲、乙两组同学将与B元素同主族的砷元素的化合物按反应“AsO
(6)下图Ⅰ、Ⅱ分别是甲、乙两组同学将与B元素同主族的砷元素的化合物按反应“AsO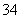 +2I-+2H+
+2I-+2H+ AsO
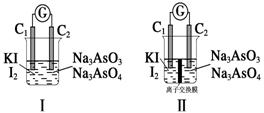
AsO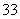 +I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸或40% NaOH溶液,电流表指针都不发生偏转;乙组经思考后先添加了一种离子交换膜,然后向图Ⅱ烧杯右侧中逐滴加入适量40%NaOH溶液,发现电流表指针发生偏转。
+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸或40% NaOH溶液,电流表指针都不发生偏转;乙组经思考后先添加了一种离子交换膜,然后向图Ⅱ烧杯右侧中逐滴加入适量40%NaOH溶液,发现电流表指针发生偏转。
① 甲组电流表指针都不发生偏转的原因是 。
② 乙组添加的是 (填“阴”或“阳”)离子交换膜。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+F2(g) === 2HF(g) △H=-270kJ/mol,下列说法正确的是( )
A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.2mol氟化氢气体分解成1mol的氢气和1mol的氟气放出270kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应PCl3g)+Cl2(g) 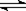 PCl5(g) 达到平衡时,PCl5为0.4mol,如果此时移走1.0mol PCl3和0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
PCl5(g) 达到平衡时,PCl5为0.4mol,如果此时移走1.0mol PCl3和0.50mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
A.0.40mol B.0.20mol C. 大于0.20mol,小于0.40mol D. 小于0.20mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中一定能大量共存的是( )
A.25 ℃时, pH=12的无色溶液:K+、Br-、SO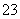 、SiO
、SiO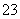
B.与铝粉反应放出氢气的溶液:HCO 、K+、Na+、SO
、K+、Na+、SO
C.使石蕊溶液显红色的溶液:Na+、NH 、Cl-、S2O
、Cl-、S2O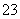
D.25 ℃时,由水电离出来的c(H+)=1×10-13 mol/L的溶液:Ba2+、Cl-、AlO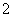 、NO
、NO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com