
分析 (1)①NaHCO3属于强碱弱酸的酸式盐,在溶液中HCO3-的水解程度大于电离程度;水解显碱性;
②NaHCO3溶液中HCO3-水解浓度减小,钠离子不水解,所以;
(2)盐的水解反应属于吸热反应,加热促进水解.
解答 解:(1)①NaHCO3属于强碱弱酸的酸式盐,在溶液中HCO3-的水解程度大于电离程度,水解显碱性,其水解方程式为:HCO3-+H2O?OH-+H2CO3;
故答案为:碱;HCO3-+H2O?OH-+H2CO3;
②HCO3-水解浓度减小,溶液中C(Na+)>C(HCO3-),故答案为:>;
(2)盐的水解反应属于吸热反应,加热促进水解,用Na2CO3溶液清洗油污时,加热促进水解溶液的碱性增强,溶液pH增大,故答案为:促进.
点评 本题考查了盐的水解原理,题目涉及水解离子方程式的书写、水解原理的应用、影响水解的因素等,题目难度不大,注意对基础知识的积累.


科目:高中化学 来源: 题型:解答题
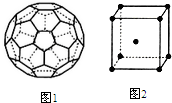 X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子.回答下列问题:
X、Y、Z、W、Q五种元素的原子序数依次增大,X、Y、Z、W属于短周期元素.已知X位于周期表的s区,其原子中电子层数和未成对电子数相同;Y原子核外有三个能级,且每个能级上容纳的电子数相同;W原子最外层电子数是次外层电子数的3倍;Q元素的原子核外有26个运动状态完全不相同的电子.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
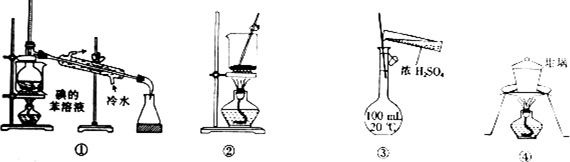
| A. | 用装置①分离碘并回收苯 | |
| B. | 用装置②灼烧海带灰 | |
| C. | 用装置③配置一定物质的量浓度的H2SO4溶液 | |
| D. | 用装置④蒸发浓缩MgCl2溶液制取MgCl2•6H2O晶体 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:填空题
化学学习中要注意对过程的分析,按要求回答下列问题:
(1)向石蕊试剂中通入氯气,起始时溶液变红,一段时间后溶液褪色,则使溶液变红和褪色的微粒分别是 、 。
(2)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液到中性,写出发生反应的离子方程式 ;在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.石灰石与盐酸反应:CO32- +2H+==H2O+CO2↑
B.醋酸与烧碱溶液反应: H++OH-==H2O
C.MgSO4溶液与Ba(OH)2溶液反应:SO42-+Ba2+= BaSO4↓
D.硫酸与氨水混合: H++NH3·H2O==NH4++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3(Al2O3)用盐酸 | B. | Fe2O3(Al2O3)用氨水 | ||
| C. | Mg(Al)用纯碱溶液 | D. | MgCl2(AlCl3)用氢氧化钠溶液和盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com