
| A、合金最多只能含有两种元素 |
| B、多数合金的硬度较大 |
| C、多数合金的熔点比成分金属低 |
| D、合金的性能跟合金元素的种类有关 |


科目:高中化学 来源: 题型:
| A、酸式盐的水溶液一定显碱性 |
| B、醋酸铵溶液呈中性是因为溶液中H+的物质的量和OH-的物质的量相等 |
| C、NaHSO3溶液的PH大于Na2SO4溶液的PH |
| D、只要酸与碱的物质的量浓度和体积分别相等,它们反应后的溶液就呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、重金属盐中毒的病人服用鸡蛋清解毒 |
| B、高温消毒医疗器械 |
| C、用甲醛的水溶液保存标本 |
| D、把生理盐水静脉注射到人体内 |
查看答案和解析>>
科目:高中化学 来源: 题型:
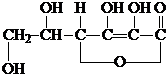 2014年8月28日,第二届夏季青年奥林匹克运动会(以下简称“青奥会”)在南京奥体中心顺利闭幕.请完成下列与“青奥会”有关的填空.
2014年8月28日,第二届夏季青年奥林匹克运动会(以下简称“青奥会”)在南京奥体中心顺利闭幕.请完成下列与“青奥会”有关的填空.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中键能越大,键长越长,则分子越稳定 |
| B、水分子可表示为H-O-H,分子中键角为180. |
| C、H-O键键能为463KJ/mol,即18gH2O分解成H2和O2时消耗能量为2×463KJ |
| D、元素周期表中的第ⅠA族和第ⅦA族元素的原子间可以形成共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+、Na+、NO3-、Br- |
| B、K+、Na+、SO32-、S2- |
| C、K+、Na+、AlO2-、SO42- |
| D、NH4+、Cu2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
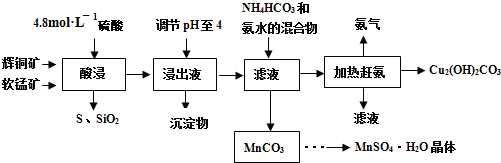
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com