
分析 在2CuFeS2+O2═□+2FeS+SO2中,先由质量守恒推断方框中的物质,再由Cu元素的化合价降低,O元素的化合价降低,S元素的化合价升高,以此来解答.
解答 解:(1)由质量守恒定律可知,Cu、S原子守恒,则方框中的物质应为Cu2S,故答案为:Cu2S;
(2)2CuFeS2+O2=Cu2S+2FeS+SO2反应中化合价升高的只有S元素,从-2价升高到+4价,若有1molSO2生成,则反应中转移的电子为1mol×(4-(-2))=6mol,故答案为:6mol;
(3)S元素由-1价升高到+4价,O元素0价降低为-2价,则SO2既是氧化产物又是还原产物,故答案为:氧化产物又是还原产物.
点评 本题考查氧化还原反应,明确元素的化合价是解答本题的关键,准确判断CuFeS2中是学生解答在的难点和易错点,难度中等.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:选择题
| A. | 阴离子: | B. | 氧化物:XOn | C. | 气态氢化物:HnX | D. | 含氧酸:HnXO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2、S、Br2 | B. | Na、金刚石、NaCl | C. | H2O、H2S、H2Se | D. | CO2、KCl、SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 CaO NaCl CBr4 CF4 | |
| B. | SiO2 NaCl CaO CF4 CBr4 | |
| C. | CaO NaCl SiO2 CBr4 CF4 | |
| D. | CF4CBr4NaCl CaO SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该反应是复分解反应 | B. | MnO2是氧化剂 | ||
| C. | HCl是还原剂 | D. | Cl2是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
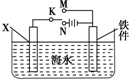 钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.
钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com