
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl﹣、CO32﹣、SO42﹣ , 现取两份100mL溶液进行如下实验: ①第一份加过量NaOH溶液加热后,只收集到气体0.02mol,无沉淀生成,同时得到溶液甲.
②在甲溶液中通入过量CO2 , 生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02g.
③第二份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65g.
根据上述实验回答:
(1)一定不存在的离子是 , 不能确定是否存在的离子是 .
(2)试确定溶液中肯定存在的离子及其浓度(可不填满): 离子符号 , 浓度;
离子符号 , 浓度;
离子符号 , 浓度 .
(3)试确定K+是否存在(填“是”或“否”),判断的理由是 .
(4)设计简单实验验证原溶液中可能存在的离子 .
【答案】
(1)Fe3+、Mg2+、CO32﹣、Ba2+;Cl﹣
(2)SO42﹣;0.5mol/L;NH4+;0.2mol/L;Al3+;0.2mol/L
(3)是;溶液中肯定存在的离子Al3+、NH4+、SO42﹣ , 经计算Al3+、NH4+物质的量都是0.02mol,SO42﹣物质的量是0.05mol,根据电荷守恒,K+一定存在
(4)取少量原溶液于试管中,向其中加入足量的硝酸钡溶液,过滤后,向滤液中加入硝酸酸化的硝酸银溶液,有白色沉淀生成证明存在氯离子
【解析】解:①第一份加过量NaOH溶液加热后,只收集到气体0.02mol,该气体是氨气,一定有铵根离子,铵根离子的物质的量是0.02mol,无沉淀生成,一定不含Fe3+、Mg2+;②在甲溶液中通入过量CO2 , 生成白色沉淀,该沉淀是氢氧化铝,沉淀经过滤、洗涤、灼烧,得到氧化铝,氧化铝质量为1.02g,即0.01mol,根据铝元素守恒,含有铝离子的物质的量是0.02mol,一定不含CO32﹣ , ③第二份加足量BaCl2溶液后,得白色沉淀,即硫酸钡沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65g,所以一定有SO42﹣ , 物质的量是 ![]() =0.05mol,一定不含Ba2+ , n(NH4+)+3n(Al3+)=0.02mol+3×0.02mol=0.08mol,2n(SO42﹣)=0.1mol,根据电荷守恒,一定存在钾离子,因为不确定的是Cl﹣ , 钾离子的最小物质的量是0.02mol, 综上 知道,一定不存在的离子有:Fe3+、Mg2+、CO32﹣、Ba2+ , 一定存在的离子有:K+、SO42﹣、NH4+、Al3+ , 不能确定的是Cl﹣ . (1)一定不存在的离子是Fe3+、Mg2+、CO32﹣、Ba2+ , 不能确定的是Cl﹣ , 所以答案是:Fe3+、Mg2+、CO32﹣、Ba2+ , Cl﹣;(2)肯定存在的离子是K+、SO42﹣、NH4+、Al3+ , NH4+的物质的量是0.02mol,体积是0.1L,所以c(NH4+)=0.2mol/L,SO42﹣物质的量是0.05mol,体积是0.1L,所以c(SO42﹣)=0.5mol/L,Al3+的物质的量是0.02mol,体积是0.1L,所以c(Al3+)=0.2mol/L,钾离子的浓度随着氯离子而定,即c(K+)≥0.2mol/L
=0.05mol,一定不含Ba2+ , n(NH4+)+3n(Al3+)=0.02mol+3×0.02mol=0.08mol,2n(SO42﹣)=0.1mol,根据电荷守恒,一定存在钾离子,因为不确定的是Cl﹣ , 钾离子的最小物质的量是0.02mol, 综上 知道,一定不存在的离子有:Fe3+、Mg2+、CO32﹣、Ba2+ , 一定存在的离子有:K+、SO42﹣、NH4+、Al3+ , 不能确定的是Cl﹣ . (1)一定不存在的离子是Fe3+、Mg2+、CO32﹣、Ba2+ , 不能确定的是Cl﹣ , 所以答案是:Fe3+、Mg2+、CO32﹣、Ba2+ , Cl﹣;(2)肯定存在的离子是K+、SO42﹣、NH4+、Al3+ , NH4+的物质的量是0.02mol,体积是0.1L,所以c(NH4+)=0.2mol/L,SO42﹣物质的量是0.05mol,体积是0.1L,所以c(SO42﹣)=0.5mol/L,Al3+的物质的量是0.02mol,体积是0.1L,所以c(Al3+)=0.2mol/L,钾离子的浓度随着氯离子而定,即c(K+)≥0.2mol/L
, 所以答案是:SO42﹣、0.5mol/L;NH4+、0.2mol/L;Al3+、0.2mol/L;(3)据电荷守恒,一定存在钾离子,因为n(NH4+)+3n(Al3+)=0.02mol+3×0.02mol=0.08mol,2n(SO42﹣)=0.1mol,根据电荷守恒,一定存在钾离子,
所以答案是:是;溶液中肯定存在的离子Al3+、NH4+、SO42﹣ , 经计算Al3+、NH4+物质的量都是0.02mol,SO42﹣物质的量是0.05mol,根据电荷守恒,K+一定存在;(4)不能确定的是Cl﹣ , 检验试剂可以采用硝酸酸化的硝酸银溶液,具体检验方法是:取少量原溶液于试管中,向其中加入足量的硝酸钡溶液,过滤后,向滤液中加入硝酸酸化的硝酸银溶液,有白色沉淀生成证明存在氯离子,
所以答案是:取少量原溶液于试管中,向其中加入足量的硝酸钡溶液,过滤后,向滤液中加入硝酸酸化的硝酸银溶液,有白色沉淀生成证明存在氯离子.


科目:高中化学 来源: 题型:
【题目】如图分别是A、B两种物质的核磁共振氢谱,已知A、B两种物质都是烃类,都含有6个氢原子,试根据两种物质的核磁共振氢谱推测A、B有可能是下面的( ) 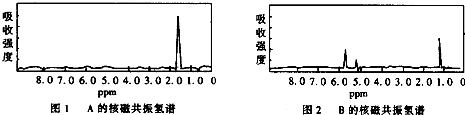
A.A是C3H6 , B是C6H6
B.A是C2H6 , B是C3H6
C.A是C2H6 , B是C6H6
D.A是C3H6 , B是C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液可能是AgNO3溶液、NaCl溶液、Na2CO3溶液和Na2SO4溶液中的一种。为检验其成分,某同学做实验如下:取少量该溶液放入试管中,加入稀盐酸酸化,无明显现象,再加入BaCl2溶液,有白色沉淀产生。上述实验说明该溶液是
A.AgNO3溶液B.NaCl溶液
C.Na2CO3溶液D.Na2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案不合理的是( )
A.除去乙醇中少量的水:加足量生石灰,蒸馏
B.分离苯和硝基苯的混合物,可用蒸馏法
C.可用苯将溴从溴苯中萃取出来
D.可用水来鉴别苯、乙醇、四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~J均为有机化合物,它们之间的转化如图所示: 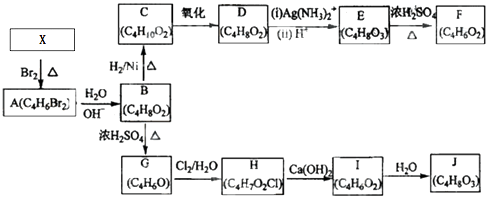
实验表明:
①D既能发生银镜反应,又能与金属钠反应放出氢气:
②核磁共振氢谱表明F分子中有三种氢,且其峰面积之比为1:1:1;
③G能使溴的四氯化碳溶液褪色;
④1mol J与足量金属钠反应可放出22.4L氢气(标准状况).
请根据以上信息回答下列问题:
(1)A的结构简式为 , 由A生成B的反应类型是反应;
(2)D的结构简式为;
(3)由E生成F的化学方程式为 , E中的官能团有(填名称),与E具有相同官能团的E的同分异构体还有(任写两个,不考虑立体结构);
(4)G的结构简式为;
(5)由I生成J的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是X河流经某工业城市Y,其中a处在上游,d处在下游。 根据2013年市环保局监测站对X河水质检测结果绘制的简图如图2所示。请据图示回答下列问题: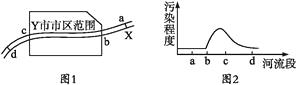
(1)造成X河水质污染的主要污染源最可能分布在( )
A.ab段
B.bc段
C.cd段
D.bd段
(2)列举造成X河污染的三种可能的污染源。
(3)若对c处水样进行检测,发现其中含有Cu2+等重金属离子。若要把铜离子变为单质铜回收,请回答两种回收的方法: 方法Ⅰ:
方法Ⅱ:
(4)d处的污染程度明显降低,请从物理学、化学、生物学三方面简单说明其原因。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛是金属中的新秀,具有质轻、高强、耐蚀、耐热、无磁和耐超低温等一系列优良性能,以及形状记忆、超导、储氢、生物相容性等四大独特功能.含有Fe2O3的钛铁矿(主要成分为FeTiO3)制取TiO2的流程如下: 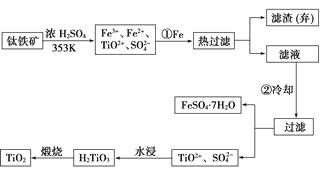
(1)Ti的原子序数为22,Ti位于元素周期表中第周期,第族.
(2)步骤①加铁的目的是;步骤②冷却的目的是.
(3)上述制备TiO2的过程中,可以利用的副产物是;考虑成本和废物综合利用因素,废液中应加入处理.
(4)由金红石(TiO2)制取单质Ti,涉及到的步骤为: TiO2―→TiCl4![]() Ti
Ti
已知:①C(s)+O2(g)===CO2(g);ΔH=-393.5kJ/mol
②2CO(g)+O2(g)===2CO2(g);ΔH=-566kJ/mol
③TiO2(s)+2Cl2(g)===TiCl4(s)+O2(g);ΔH=+141kJ/mol
则TiO2(s)+2Cl2(g)+2C(s)===TiCl4(s)+2CO(g)的ΔH=.
反应TiCl4+2Mg===2MgCl2+Ti在Ar气氛中进行的理由是.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是用途最广的金属材料之一.为探究铁的化学性质,某同学将盛有生铁屑的试管塞上蓬松的棉花,然后倒置在水中(如图所示).数天后,他观察到的现象是( )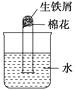
A.铁屑不生锈,试管内液面上升
B.铁屑不生锈,试管内液面高度不变
C.铁屑生锈,试管内液面上升
D.铁屑生锈,试管内液面高度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.物质发生化学反应都伴随着能量变化
B.伴有能量变化的物质变化都是化学变化
C.在吸热反应中,反应物的总能量高于生成物的总能量
D.需要加热的化学反应一定是放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com