
分析 (1)结合方程式计算被氧化的HI的量;
(2)根据反应时有沉淀、气体、颜色变化等明显现象选择试剂;
(3)使NaNO2转化为不引起二次污染的N2,N元素的化合价降低,则选择还原剂,以此来解答.
解答 解:(1)设被氧化的HI的物质的量为x,
2NaNO2+4HI═2NO+I2+2NaI+2H2O
2 4
1.5mol x
所以$\frac{2}{1.5}=\frac{4}{x}$
x=3mol;
故答案为:3l;
(2)①自来水、③淀粉、④白糖、⑥白酒与NaNO2都不反应,所以无明显现象;
KI与NaNO2反应生成I2必须在酸性条件下才能反应,食醋会电离出微量的氢离子,碘化钾在食醋本身带的溶剂水中电离出碘离子,
亚硝酸钠电离出亚硝酸根与钠离子,发生反应生成碘单质,I2使湿润的淀粉碘化钾试纸变蓝,
故答案为:②;
(3)使NaNO2转化为不引起二次污染的N2,N元素的化合价降低,则选择还原剂,只有NH4Cl 符合,发生反应为NH4Cl+NaNO2=NaCl+N2+2H2O,
故答案为:②;NH4Cl+NaNO2=NaCl+N2+2H2O.
点评 本题考查的是氧化还原反应的有关计算及试剂的选择,鉴别物质选择试剂时,选择的试剂 反应时有明显变化现象才行.本题还是一个信息给予题,信息给予题着重考查学生临场阅读,提取信息和进行信息加工、处理的能力,以及灵活运用基础知识分析问题、解决问题的综合能力.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:解答题
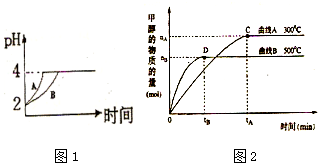 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入HBr | B. | 加入NaCO3溶液 | C. | 加入NaBr | D. | 加入Na2SO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
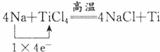 ,氧化剂:TiCl4,还原剂:Na.
,氧化剂:TiCl4,还原剂:Na.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 5H3AsO4+4Br2+4K2SO4+4H2O.
5H3AsO4+4Br2+4K2SO4+4H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4在熔融的状态下能够导电是因为:NaHSO4═Na++HSO4- | |
| B. | pH=1的无色溶液中能大量共存的离子有:CO32-、Na+、Cl-、Ba2+ | |
| C. | 能用Fe3++3OH-=Fe(OH)3↓表示的化学方程式可以是:2Fe(NO3)3+3Mg(OH)2═2Fe(OH)3↓+3Mg(NO3)2 | |
| D. | 铜片和稀HNO3反应离子方程式为:Cu+4H++NO3-═Cu2++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂是SiO2 | |
| B. | 氧化剂与还原剂的物质的量之比为1:2 | |
| C. | 由反应可得C的还原性比Si强 | |
| D. | 若生成1 mol SiC,则转移电子2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
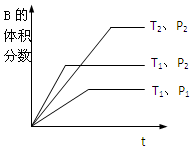 (1)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)在一定温度下,将2molA和2molB两种气体相混合后于容积为2L的某密闭容器中,发生如下反应3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com