
氮化铝(AlN)广泛应用于电子,陶瓷等工业领域,在一定的条件下,AlN可通过反应
 Al2O3+N2+3C 2 AlN+3CO合成,下列叙述正确的是 ( )
Al2O3+N2+3C 2 AlN+3CO合成,下列叙述正确的是 ( )
A.上述反应中,N2是还原剂,Al2O3是氧化剂;
B.上述反应中,每生成1mol AlN,需转移3 mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41g
科目:高中化学 来源: 题型:
对于反应2NO2(g) N2O4(g)达到平衡后,在温度不变时欲使c(NO2)/c(N2O4)比值增大,可以采取( )
N2O4(g)达到平衡后,在温度不变时欲使c(NO2)/c(N2O4)比值增大,可以采取( )
A. 体积不变,增加NO2的量 B. 体积不变,增加N2O4的量
C. 使体积扩大到原来的2倍 D. 使体积不变充入N2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列气体干燥时所选干燥剂(括号内为干燥剂)正确的是( )
A. Cl2(碱石灰) B. SO2(生石灰)
C. NH3(无水硫酸铜) D. HCl(氯化钙或五氧化二磷)
查看答案和解析>>
科目:高中化学 来源: 题型:
锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成1 mol硝酸锌时,被还原的硝酸的物质的量为
A.2 mol B.1 mol C.0.5 mol D.0.25 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
2 g Cu2S和CuS的混合物在酸性溶液中用400 mL 0.075 mol·L-1 KMnO4溶液处理,发生反应如下:
8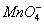 +5Cu2S+44H+====12Cu2++5SO2+8Mn2++22H2O
+5Cu2S+44H+====12Cu2++5SO2+8Mn2++22H2O
6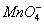 +5CuS+28H+====5Cu2++5SO2+6Mn2++14H2O
+5CuS+28H+====5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:

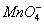 +
+ Fe2++
Fe2++ H+
H+ Mn2++
Mn2++ Fe3++
Fe3++ H2O
H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为_________mol。
(3)欲配制500 mL 0.1 mol·L-1 Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392 g·mol-1)的质量为_________ g。
(4)混合物中Cu2S的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求ClO2将逐渐取代Cl2成为生产自来水消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,在以上反应中NaClO3和Na2SO3的物质的量之比为 ( )
A.1:1 B.2:1
C.1:2 D.2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
 下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
| a | b | c | |
| A | Al | AlCl3 | Al(OH)3 |
| B | HNO3 | NO | NO2 |
| C | Si | SiO2 | H2SiO3 |
| D | CH2=CH2 | CH3CH2OH | CH3CHO |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语正确的是
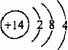
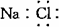 A.氯化钠的电子式: B.乙烯的结构简式:C2H4
A.氯化钠的电子式: B.乙烯的结构简式:C2H4
C.硅的原子结构示意图: D.硫酸的电离方程式:Na2SO4=Na2++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
在400 ℃、101 kPa,将SO2和14 mol O2装入一个有催化剂的5 L密闭容器中,发生了2SO2(g)+O2(g)  2SO3(g)的反应,10 min时达到平衡时,测得容器内有2 mol SO2和12 mol O2 。则:(提示:用三步法)
2SO3(g)的反应,10 min时达到平衡时,测得容器内有2 mol SO2和12 mol O2 。则:(提示:用三步法)
(1)SO2的起始浓度
(2)平衡体系中含SO3的体积分数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com