
在固定体积的密闭容器中进行如下反应:2AB2(g)+B2(g) 2AB3(g)。已知反应过程某一时刻AB2、B2、AB3浓度分别为0.2 mol/L、0.1 mol/L、0.2
mol/L,达到平衡时,浓度可能正确的是
2AB3(g)。已知反应过程某一时刻AB2、B2、AB3浓度分别为0.2 mol/L、0.1 mol/L、0.2
mol/L,达到平衡时,浓度可能正确的是
A. AB2、B2分别为0.4mol/L、0.2mol/L
B. AB2为0.25mol/L
C. AB2、AB3均为0.15mol/L
D. AB3为0.4mol/L
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:

c(N
| ||
| c(NH3?H2O) |
| c(NH3?H2O) |
| c(OH-) |
| c(OH-) |
| c(H+) |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AB2、B2分别为0.4mol/L、0.2mol/L | B、AB2为0.25mol/L | C、AB2、AB3均为0.15mol/L | D、AB3为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
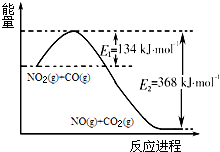 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2为0.4mol/L | B、SO2为0.25mol/L | C、O2为0.2mol/L | D、O2为0mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com