
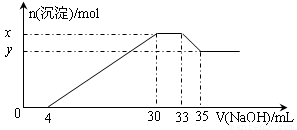
在200 mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是( )
A.原溶液中n(Mg2+)∶n(Al3+)=10∶1
B.原溶液的c(H+)=0.8 mol/L
C.x与y的差值为0.01 mol
D.原溶液中c(Cl-)=0.66mol/L
D
【解析】
试题分析:由图象可知,开始加入氢氧化钠没有沉淀生成,0~4mL发生反应H++OH-=H2O,4mL时H +反应完毕,4~30mL发生反应Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,30mL时沉淀量最大,Mg2+、Al3+沉淀完全,30~33mL沉淀量不变,发生NH4+与氢氧化钠的反应NH4++OH-=NH3·H2O,33~35mL发生Al(OH)3与氢氧化钠的反应Al(OH)3+OH-=AlO2-+2H2O,0~4mL发生H+与氢氧化钠的反应,则H+的物质的量为4mL×10-3L×4mol?L-1=0.016mol,c(H+)=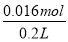 =0.08mol/L,故B错误;由图象可知,x与y的差值即为Al(OH)3的物质的量,由Al(OH)3+NaOH=NaAlO2+2H2O,NaOH的物质的量为(35-33)mL×10-3L×4mol?L-1=0.008mol,即Al(OH)3的物质的量=0.008mol,故C错误;溶液中的阴离子只有Cl―,则加入33mLNaOH溶液时Cl―全部存在于NaCl中,则Cl―的物质的量为33mL×10-3L×4mol?L-1=0.132mol,原溶液中c(Cl―)=
=0.08mol/L,故B错误;由图象可知,x与y的差值即为Al(OH)3的物质的量,由Al(OH)3+NaOH=NaAlO2+2H2O,NaOH的物质的量为(35-33)mL×10-3L×4mol?L-1=0.008mol,即Al(OH)3的物质的量=0.008mol,故C错误;溶液中的阴离子只有Cl―,则加入33mLNaOH溶液时Cl―全部存在于NaCl中,则Cl―的物质的量为33mL×10-3L×4mol?L-1=0.132mol,原溶液中c(Cl―)=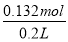 =0.66mol/L,故D正确;由C计算可知n[Al(OH)3]=0.008molmol,则原溶液中n(Al3+)=n[Al(OH)3]=0.008mol,由图可知溶解Al(OH)3消耗氢氧化钠溶液5mL,则沉淀Mg2+、Al3+消耗氢氧化钠溶液26mL,则n(NaOH)=(30-4)mL×10-3L×4mol?L-1=0.104mol,根据氢氧根守恒该阶段有3n[Al(OH)3]+2n[Mg(OH)2]=n(NaOH),则n[Mg(OH)2]=
=0.66mol/L,故D正确;由C计算可知n[Al(OH)3]=0.008molmol,则原溶液中n(Al3+)=n[Al(OH)3]=0.008mol,由图可知溶解Al(OH)3消耗氢氧化钠溶液5mL,则沉淀Mg2+、Al3+消耗氢氧化钠溶液26mL,则n(NaOH)=(30-4)mL×10-3L×4mol?L-1=0.104mol,根据氢氧根守恒该阶段有3n[Al(OH)3]+2n[Mg(OH)2]=n(NaOH),则n[Mg(OH)2]= 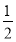 (0.104mol-0.008mol×3)=0.04mol,故原溶液中n(Mg2+)=0.04mol,故原溶液中n(Mg2+):n(Al3+)=5:1,故A错误;
(0.104mol-0.008mol×3)=0.04mol,故原溶液中n(Mg2+)=0.04mol,故原溶液中n(Mg2+):n(Al3+)=5:1,故A错误;
考点:查化学反应图象及离子反应计算。


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源:2012年普通高等学校招生全国统一考试化学(山东卷解析版) 题型:实验题
(14分)(2012?山东)实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:
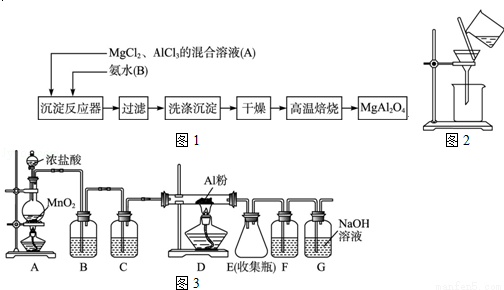
(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入 (填“A”或“B”),再滴加另一反应物.
(2)如下图所示,过滤操作中的一处错误是 .
(3)判断流程中沉淀是否洗净所用的试剂是 .高温焙烧时,用于盛放固体的仪器名称是 .
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备.
装置B中盛放饱和NaCl溶液,该装置的主要作用是 .F中试剂的作用是 .用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为 .
查看答案和解析>>
科目:高中化学 来源:2012-2014四川省宜昌市春季期中考试高一化学试卷(解析版) 题型:选择题
下列各种说法中,正确的是 ( )
A.3号到9号元素化合价的变化与11到17号元素化合价的变化完全相同
B.同周期原子半径逐渐减小,所以离子半径也逐渐减小
C.随着原子序数的递增,碱金属元素单质的还原性逐渐增强,阳离子的氧化性逐渐减弱
D.甲乙电子层数相同,甲的最高价氢氧化物的碱性比乙的最高价氢氧化物的碱性强,说明甲的核电荷数比乙大
查看答案和解析>>
科目:高中化学 来源:2012-2013陕西省富平县高一下学期期末考试化学试卷(解析版) 题型:选择题
等质量的下列有机物完全燃烧,消耗O2最多的是 ( )
A.CH4B.CH3CH3C.C2H2D.C5H12
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高一上学期期末化学试卷(解析版) 题型:填空题
(1)写出工业用纯碱、石灰石、石英制普通玻璃的化学方程式 ; 。
(2)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。原因是 (用化学方程式表式)
(3)向100ml水中投入Na和Al共16克,充分反应后分析剩余金属1g。计算放出H2的体积为 升(标准状况下)
(4)向含有0.3mol的NaAlO2溶液中滴加1mol/L HCl,当生成7.8克沉淀时,加入盐酸的体积为 mL
(5)向一定量的Fe、Fe2O3和CuO混合物投入120 ml 2.2 mol/L的硫酸溶液中,充分反应后生成896 mL标准状况下的气体,得不溶物1.28 g,过滤后,向滤液中加入2 mol/L的NaOH溶液,加至40 mL时开始出现沉淀,则滤液中FeSO4的物质的量浓度为(设滤液体积为120 ml) mol/L
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高一上学期期末化学试卷(解析版) 题型:选择题
下列溶液中Cl-浓度最大的是( )
A.10ml 0.2mol/L的FeCl3溶液
B.10ml 0.1mol/L的AlCl3溶液
C.20ml 0.1mol/L的MgCl2溶液
D.20ml 0.1mol/L的HCl溶液
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高一上学期期末化学试卷(解析版) 题型:选择题
用NA代表阿伏加德罗常数,下列说法正确的是( )
A.1molO2作为氧化剂得到的电子数一定为4NA
B.在标准状况下,11.2L水中含有分子数为0.5NA
C.0.4mol/LNa2SO4溶液中,所含Na+和SO42―总数为1.2NA
D.标准状况下,40gSO3所占的体积一定小于11.2L。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列各物质,所含原子数目最多的是( )
A.标准状况下,22.4L甲烷
B.标准状况下,44.8L氮气和氧气的混合气体
C.常温常压下,66g二氧化碳气体
D.100mL 1mol/L硫酸
查看答案和解析>>
科目:高中化学 来源:2016届重庆市高一上学期期中考试化学试卷(解析版) 题型:填空题
现有以下物质:①Al;②稀硫酸;③NaHCO3;④液氨;⑤盐酸;⑥蔗糖溶液;⑦无水乙醇;⑧熔融NaOH;⑨NaHSO4;⑩CO2,回答下列问题(用相应物质的序号填写)
(1)可以导电的有 ;
(2)属于非电解质的有 ;
(3)请写出③的电离方程式 ;
(4)写出⑧中的物质的溶液与⑨的溶液反应的离子方程式 ;
(5)写出①与⑧中的物质的溶液反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com