
已知反应:①101kPa时,C(s)+ O2(g)═CO(g)△H1=-110.5kJ/mol
O2(g)═CO(g)△H1=-110.5kJ/mol
②稀溶液中:H+(aq)+ OH-(aq )═H2O(l) △H2=-57.3kJ/mol
下列说中正确的是
A、若碳的燃烧热用△H3表示,则△H3<△H1
B、若碳的燃烧热用△H3来表示,则△H3>△H1
C、浓硫酸与稀NaOH溶液反应的中和热值为57.3kJ·mol-1
D、稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ的热量
 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源:2015届江西省高三上学期第一学期月考化学试卷(解析版) 题型:选择题
下列有关试验的做法不正确的是
A. 用加热分解的方法区分碳酸钠和碳酸氢钠两种固体
B.配置0.1000 mol·L-1氢氧化钠溶液时,将液体转移到容量瓶中需用玻璃棒引流
C. 检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体
D.分液时,分液漏斗的顶塞应打开或使塞上凹槽与壁上小孔对准
查看答案和解析>>
科目:高中化学 来源:2015届江苏省苏州市高三9月学情调研化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.核内有8个中子的碳原子: B.甲烷分子的比例模型:
B.甲烷分子的比例模型:
C.羟基的电子式: D.氯离子的结构示意图:
D.氯离子的结构示意图:
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市协作体高二下学期期中考试化学试卷(解析版) 题型:选择题
可以证明可逆反应N2 + 3H2 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
①一个N≡N断裂的同时,有3个H-H键断裂;②一个N≡N键断裂的同时,有6个N-H键断裂;③其它条件不变时,混合气体平均相对分子质量不再改变;④保持其它条件不变时,体系压强不再改变;⑤NH3、N2、H2的体积分数都不再改变;⑥恒温恒容时,混合气体的密度保持不变;⑦正反应速率v(H2) = 0.6 mol/(L·min),逆反应速率v(NH3) = 0.4 mol/(L·min)
A.全部 B.①③④⑤ C.②③④⑤⑦ D.③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市协作体高二下学期期中考试化学试卷(解析版) 题型:选择题
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应为:2CH3OH+3O2+4OH- 2CO32-+6H2O,则下列有关说法不正确的是
2CO32-+6H2O,则下列有关说法不正确的是
A、放电时化学能转变为电能 B、放电时CH3OH参与正极反应
C、充电时阴极产生CH3OH D、充电时每生成1mol CH3OH,则转移6mol电子
查看答案和解析>>
科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:填空题
(18分)已知可逆反应CO2(g) + H2(g) CO(g) + H2O(g),
CO(g) + H2O(g),
⑴写出该反应的化学平衡常数表达式:K= 。
⑵830K时,若起始时:c (CO2)=2mol/L,c (H2)=3mol/L,平衡时CO2的转化率为60%,氢气的转化率为 ;K值为 。
⑶830K时,若只将起始时c (H2)改为6mol/L,则氢气的转化率为 。
⑷若830K时,起始浓度c (CO2) = a mol/L,c (H2) = b mol/L,H2O的平衡浓度为c (H2O) = c mol/L,则:①a、b、c之间的关系式是 ;②当a = b时,a = c。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省沭阳县高二下学期期中调研测试化学试卷(解析版) 题型:选择题
已知25℃、101kPa条件下:
4Al (s) + 3O2 (g)=2Al2O3 (s) △H=-2834.9 kJ/mol
4Al (s) + 2O3 (g) = 2Al2O3 (s) △H= -3119.91kJ/mol
由此得出的结论正确的是
A.等质量的O2比O3能量低,由O2变O3 为放热反应
B.等质量的O2比O3能量低,由O2变O3 为吸热反应
C.3O2(g)=2O3 (g) △H=285.0 kJ/mol
D.O3比O2稳定,由O2变O3 为吸热反应
查看答案和解析>>
科目:高中化学 来源:2015届江苏省无锡江阴市高二下学期期中考试化学试卷(解析版) 题型:填空题
(1)已知下列两个热化学方程式:
C3H8(g)+5O2(g) =3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
则0.5 mol丙烷燃烧生成CO2和气态水时释放的热量为 。
(2)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式: 。
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN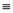 N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出 kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出 kJ能量。

(4)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:2H2+O2=2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将 能转化为 能。其电极反应式分别为:负极 ,正极 。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期摸底考试化学试卷(解析版) 题型:填空题
(12分)铁在地壳中的含量约占 5 %左右。铁矿石的种类很多,重要的有磁铁矿石
(主要成分是Fe3O4)、赤铁矿石(主要成分是 Fe2O3)等。
(1)红热的铁能跟水蒸气反应,一种产物与磁铁矿的主要成分相同,另一种产物是
可燃性气体,则其反应的化学方程式为 。 该可燃气体在酸性
条件下,可制成燃料电池,写出该气体发生的电极反应式 。
(2)在常温下,铁跟水不起反应。但在潮湿的空气中,铁很容易生锈(铁锈的主要成分是 Fe203)而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。铁生锈的化学原理如下,请你用离子方程式和化学方程式补充完整。
① 原电池反应:
负极:2Fe-4e-=2Fe2+、正极: ;
② 氢氧化物的形成: Fe2 + + 2OH-= Fe(OH) 2↓ 。
③ 氢氧化物的分【解析】
2Fe(OH)3 =Fe2O3+3H2O。
(3)为了防止铁生锈,可在铁制品表面镀上一层铜(如图装置),a为 (填“正极”或“负极”),
铁制品表面发生的电极反应式 为 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com