
| ���� |
| ���� |
| ���� |
| 27.6g |
| (100x+84y)g/mol |
| 27.6y |
| 100x+84y |
| 27.6y |
| 100x+84y |
| 6.72L |
| 22.4L/mol |
| ||
| 100x+84y |
| 2.76g |
| 44(x+y) |
| 1.32g |
| ||
| ���� |
| ���� |
| ||
| VL |
| 22.4L/mol |
| 184 |
| mag |
| 6��28 |
| 1.25Vg |


 �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��Ȼ�������һ�ְ���ʯ�Ŀ�ʯ���仯ѧʽ��xCaCO3?yMgCO3������Ϊԭ�ϣ�����ȡ�ͻ���ϵȣ�
��Ȼ�������һ�ְ���ʯ�Ŀ�ʯ���仯ѧʽ��xCaCO3?yMgCO3������Ϊԭ�ϣ�����ȡ�ͻ���ϵȣ�| ���� |
| ���� |
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡͨ����ʯ����ѧ2008�������ѧ��Ԥ��� ���ͣ�038
��Ȼ�������һ�ְ���ʯ�Ŀ�ʯ���仯ѧʽ��xCaCO3��yMgCO3������Ϊԭ�ϣ�����ȡ�ͻ���ϵȣ�
(1)��ȡ27.6 g����ʯ�����ȵ��������ٱ仯�����������ͻ����MgO����mol��(��x��y�Ĵ���ʽ��ʾ)
(2)����������Ӧ�У��ռ���CO2��6.72 L(��״����)����д������ʯ�Ļ�ѧʽ(ȡx��y����С��������)��
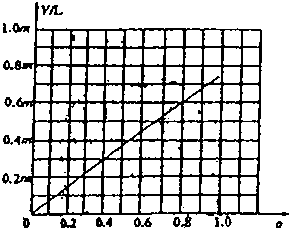
(3)����ȡ����ʯmg������������̿�ۻ�ϣ������ض������и�������ǿ��һ��ʱ���ð���ʯ�ֽ���Ϊa������VL(��״��)һ����̼���Լ���VΪ����L(��״��)��(��m��a����ʽ��ʾ)
(��֪CaO��3C![]() CaC2��CO��
CaC2��CO��
2MgO��5C![]() Mg2C3��2CO)
Mg2C3��2CO)
������ͼ�л���V��a�Ĺ�ϵͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011�꽭��ʡ�����������ݼ��ѧУ�߿���ѧһģ�Ծ��������棩 ���ͣ������
 CaC2+CO
CaC2+CO Mg2C3+2CO
Mg2C3+2CO 2CO��
2CO��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com