
用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解Al2O3的离子方程式是________________________________________________________________________
________________________________________________________________________。
(2)将MnO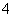 氧化Fe2+的离子方程式补充完整:
氧化Fe2+的离子方程式补充完整:
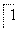 MnO
MnO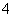 +
+ Fe2++
Fe2++ ________===
________===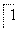 Mn2++
Mn2++ Fe3++
Fe3++ ________。
________。
(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释步骤Ⅱ的目的________________________________________________________________________。
(4)已知:一定条件下,MnO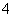 可与Mn2+反应生成MnO2。
可与Mn2+反应生成MnO2。
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是________________________________________________________________________。
②Ⅳ中加入MnSO4的目的是________________________________________________________________________。
答案 (1)Al2O3+6H+===2Al3++3H2O
(2)5 8 H+ 5 4 H2O
(3)pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)①生成黄绿色气体 ②除去过量的MnO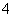
解析 (1)H2SO4溶解Al2O3的离子方程式为Al2O3+6H+===2Al3++3H2O,在操作Ⅰ中,FeO·xFe2O3也同时被溶解,滤液中含有Al3+、Fe2+、Fe3+等。
(2)步骤Ⅰ所得溶液中会有过量H2SO4,故反应在酸性条件下进行,由氧化还原反应中得失电子守恒可知MnO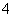 和Fe2+的化学计量数之比为1∶5,然后观察配平。得MnO
和Fe2+的化学计量数之比为1∶5,然后观察配平。得MnO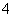 +5Fe2++8H+===Mn2++5Fe3++4H2O。
+5Fe2++8H+===Mn2++5Fe3++4H2O。
(3)步骤Ⅱ中,加入过量KMnO4溶液目的是把Fe2+氧化成易除去的Fe3+。调节pH约为3,由表中数据分析,可知该条件使Fe3+完全沉淀而Al3+不被沉淀,从而达到分离Fe3+和Al3+的目的。
(4)①联想Cl2的实验室制法,很容易分析实验设计的意图,即通过是否产生Cl2来判断沉淀中有无MnO2。②操作Ⅳ中加入MnSO4,紫红色消失,说明过量的MnO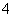 因加入MnSO4而被
因加入MnSO4而被
转化成沉淀,然后过滤除去MnO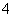 ,保证产品的纯度。
,保证产品的纯度。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同回答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。
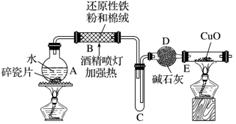
(1)硬质玻璃管B中发生反应的化学方程式为_______________________________________。
(2)反应前A中投放碎瓷片的目的是______________________________________________。
(3)装置E中的现象是___________________________________________________________。
探究二 设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于________后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变血红色,推断硬质玻璃管B中固体物质的成分为_____(选填序号,下同);若溶液未变血红色,推断硬质玻璃管B中固体物质的成分为______。
①一定有Fe3O4 ②一定有Fe
③只有Fe3O4 ④只有Fe
(6)另一份用________(填仪器名称)加入________(填试剂和现象),可以证明溶液中存在Fe2+。
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(7)试剂b的化学式是________。
(8)计算反应后B装置中铁元素的质量分数为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
石油化工专家闵恩泽院士获2007年度国家最高科学技术奖,他是石油化工技术自主创新的先行者和绿色化学的开拓者,他研制的多种石油炼制催化剂极大地降低了我国石油化工产品的成本。
(1)使用催化剂进行石油裂化获得的主要产品是________,石油裂解的主要目的是________________________________________________________________________。
(2)“绿色化学工艺”的理想状态是反应物中原子利用率为100%。工业上,通过绿色化学工艺用CO、CH3OH和一种不饱和脂肪链烃合成CH2===C(CH3)COOCH3,该不饱和脂肪链烃的分子式为________。
(3)科研人员在实验室中按下列流程在催化反应器中装载不同的催化剂,探究不同催化剂对石油裂解反应的催化性能。
 →
→ →
→ →
→
①该探究实验的条件控制非常重要,检测装置中选择的检测试剂及必须注意的问题是____________。
②从安全的角度考虑,本实验尾气处理的方法是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:将Cl2通入适量KOH溶液,产物中可能有KCl、KClO、KClO3,且 的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
的值与温度高低有关。当n(KOH)=a mol时,下列有关说法错误的是( )
A.若某温度下,反应后 =11,则溶液中
=11,则溶液中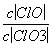 =
=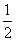
B.参加反应的氯气的物质的量等于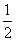 a mol
a mol
C.改变温度,反应中转移电子的物质的量ne的范围: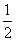 a mol≤ne≤
a mol≤ne≤ a mol
a mol
D.改变温度,产物中KClO3的最大理论产量为  a mol
a mol
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)[2014·天津理综,7(6)]KClO3可用于实验室制O2,若不加催化剂,400 ℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:________________________________________________________________________。
(2)[2014·天津理综,9(7)]Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO ,常用作脱氯剂,该反应的离子方程式为________________________________。
,常用作脱氯剂,该反应的离子方程式为________________________________。
(3)[2014·天津理综,10(1)]天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:________________________________________________________________________。
(4)(2014·上海,28)硫化氢具有还原性,可以和许多氧化剂反应。在酸性条件下,H2S和KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式。
________________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
5.6 g Cu、Mg合金与一定量的硝酸恰好完全反应,收集到NO和NO2的混合气体V L(标准状况);向反应后的溶液中加入足量NaOH溶液,沉淀完全后将其过滤、洗涤、干燥,称得质量为10.7 g。则V等于( )
A.2.24 B.4.48
C.6.72 D.7.84
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)次磷酸钠(NaH2PO2)可用于化学镀镍,即通过化学反应在塑料镀件表面沉积镍—磷合金。
化学镀镍的溶液中含有Ni2+和H2PO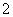 ,在酸性条件下发生以下镀镍反应:
,在酸性条件下发生以下镀镍反应:
Ni2++____H2PO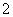 +__________—→____Ni+____H2PO
+__________—→____Ni+____H2PO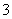 +__________
+__________
①请配平上述化学方程式。
②上述反应中,若生成1 mol H2PO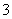 ,反应中转移电子的物质的量为________。
,反应中转移电子的物质的量为________。
(2)①高铁酸盐也是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:
2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑
②若生成2 mol Na2FeO4,则反应中电子转移的物质的量为________mol。
高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+1 mg的水体样本,需要1.2 mg·L-1高铁酸钾________ L。
(3)S2O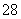 具有强氧化性,其还原产物为SO
具有强氧化性,其还原产物为SO ,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液。请写出此反应的化学方程式:________________________________________________________________________。
,硫酸锰(MnSO4)和过硫酸钾(K2S2O8)两种盐溶液在银离子催化下可发生反应,得到紫红色溶液。请写出此反应的化学方程式:________________________________________________________________________。
(4)①在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请配平该化学方程式:
FeSO4+____KNO3+____H2SO4——____K2SO4+____Fe2(SO4)3+____NO↑+____H2O;其中氧化剂为__________。
②铁红是一种红色颜料,其成分是Fe2O3,将一定量的铁红溶于160 mL 5 mol·L-1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24 L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
电解尿素[CO(NH2)2]的碱性溶液制氢气的装置示意图如下:

电解池中隔膜仅阻止气体通过,阴阳两极均为惰性电极。
(1)A极为________,电极反应式为_________________________________________。
(2)B极为________,电极反应式为______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com