
“蛟龙”号外壳用特殊的钛合金材料制成,它可以在深海中承受700个大气压的压力。已知金属钛的原子序数为22,化学性质与铝类似。下列说法正确的是
A.钛属于主族元素
B.钛合金强度很大
C.蒸干TiCl4溶液可得无水钛盐
D.在空气中将金属钛、铝混合后熔化可制得合金
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源:2014-2015广东省佛山市高一下学期第一次月考理化学试卷(解析版) 题型:计算题
(6分)浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48L(标准状况)。
试计算:
(1)反应后生成硫酸铜的物质的量。
(2)若将反应后的溶液稀释至500mL,计算该溶液中硫酸铜的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源:2014-2015广东省佛山市高二下学期第一次月考理化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.CH3—CH=CH2和CH2=CH2的最简式相同
B.CH≡CH和C6H6含碳量相同
C.乙炔和苯互为同系物
D.正戊烷、异戊烷、新戊烷的沸点逐渐降低
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市高三下学期第二次质量检测理综化学试卷(解析版) 题型:选择题
下列实验操作、现象和结论均正确的是
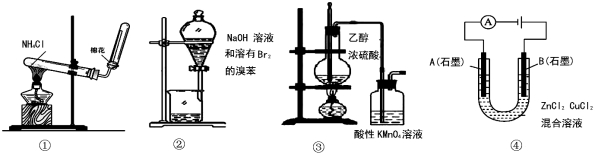
选项 | 操作 | 现象 | 结论 |
A | ①将湿润的红色石蕊试纸靠近试管口 | 试纸不变色 | NH4Cl受热不分解 |
B | ②中振荡后静置 | 下层液体颜色变浅 | NaOH溶液可除去溶在溴苯中的Br2 |
C | ③加热 | 洗气瓶中溶液褪色 | 生成了乙烯 |
D | ④通电 | B极上有红色固体析出 | 锌的金属性比铜强 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市河西区高三下学期总复习质量调查一理综化学试卷(解析版) 题型:填空题
(14分)A~I都是由短周期元素组成的常见物质,它们之间的转化关系如下图所示。已知:A为气体,其水溶液呈碱性;D、F均能与人体血液中的血红蛋白结合而使人中毒;E可作为半导体材料。
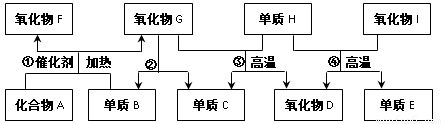
(1)化合物A的电子式为_______________________。
氧化物I中化学键类型:_____________________。
组成E单质的元素在元素周期表中的位置是____________________________。
图中物质所含元素原子的半径由大到小依次是(写元素符号)_____________。
(2)反应④的化学方程式为______________________________________________。
(3)将F与B按体积比2:1混合生成气体M,常温下测定M相对分子质量时,得到的实验值总是比理论值偏大,其原因是(用化学方程式表示)___________________。
(4)某容积为V L的试管中充满F气体(标准状况下),若将该气体完全被水吸收,需通入B的物质的量为(写含V的表达式)_______________mol,此时所得溶液中再通入气体A,恰好完全反应后所得溶液中各离子浓度由大到小依次为:_________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市和平区高三下学期第一次质量调查化学试卷(解析版) 题型:填空题
(14分)C、O、Na、Al、S、Cl是常见的六种元素。
(1)C元素位于元素周期表第 周期,第 族;C元素的一种中子数为8同位素的符号为 。
(2)用“大于”“小于”或“等于”填空
离子半径 | 酸性 | 还原性 | 得电子能力 |
N3- Al3+ | H2SO4 HClO4 | O2- S2- | 35Cl 37Cl |
(3)①CaCO3和适量HCl溶液反应时,每产生4.4 g 气体(不考虑气体溶解),放热a kJ,则该反应的热化学方程式为 。
②上述反应至无气泡逸出后,取适量残留溶液,插入pH传感器并逐滴滴入碳酸钠溶液,测得pH变化曲线如图所示。
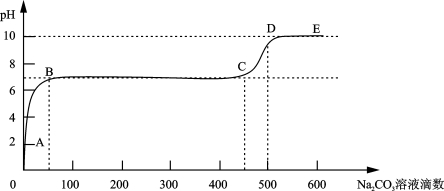
请用离子方程式表示B-C段发生的反应: 。
(4)氢气、氧气常用来作燃料电池,写出电解质为氢氧化钠溶液时负极上的电极方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省资阳市高三第三次模拟考试理综化学试卷(解析版) 题型:填空题
(14分)锌钡白是一种白色颜料。工业上是由ZnSO4与BaS溶液混合而成:BaS+ZnSO4=ZnS↓+BaSO4↓。请根据以下工业生产流程回答有关问题。

Ⅰ、ZnSO4溶液的制备与提纯:
有关资料:a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等;
b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2。
(1)②中使用的氧化剂最好是下列的 (选填字母代号)。
A.Cl2 B.浓HNO3 C.KMnO4 D.H2O2
(2)为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤 (选填①、②、③、⑤)。
(3)写出步骤④后产生滤渣3的化学式 。
(4)与Al相似,Zn也能溶于NaOH溶液。写出将Zn片和Cu片放入NaOH溶液中形成原电池的负极电极反应式: 。
Ⅱ、BaS溶液的制备:
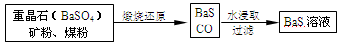
有关数据:Ba(s)+S(s)+2O2(g)=BaSO4(s) ΔH1=-1473.2 kJ·mol-1
C(s)+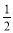 O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
Ba(s)+S(s)=BaS(s) ΔH3=-460 kJ·mol-1
(5)若煅烧还原的产物仅为BaS和CO,则其反应的热化学方程式为: 。
Ⅲ、制取锌钡白:
(6)如果生产流程步骤⑤硫酸过量,则ZnSO4与BaS溶液混合制取锌钡白产生的后果是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省渭南市高三教学质量检测(一模)化学试卷(解析版) 题型:选择题
下列有关叙述正确的是
A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1x 10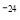 ,该溶液中一定可以大量存在K+、Na+、ClO-、SO42-。
,该溶液中一定可以大量存在K+、Na+、ClO-、SO42-。
B.对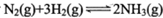 ,恒温恒容时充入N2,正反应速率增大,逆反应速率减小
,恒温恒容时充入N2,正反应速率增大,逆反应速率减小
C.已知25℃时Ksp(AgCl)=1.8×10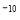 ,则在0.1 mo1
,则在0.1 mo1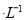 AlCl3溶液中,Ag+的物质的量浓度最大可达到6.0×10
AlCl3溶液中,Ag+的物质的量浓度最大可达到6.0×10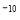 mo1
mo1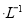 。
。
D.在酸碱中和滴定时,装标准液的滴定管未用标准液润洗直接装入标准液进行滴定,会引起测定结果浓度偏低
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一下学期第一次月考化学试卷(解析版) 题型:填空题
(9分)
(1)请用下列10种物质的序号填空:①O2 ②H2 ③NH4NO3 ④K2O2 ⑤Ba(OH)2 ⑥CH4 ⑦CO2 ⑧NaF ⑨NH3 ⑩I2
既有离子键又有非极性键的是________;既有离子键又有极性键的是________。
(2)X、Y两种主族元素能形成XY2型化合物,已知XY2中共有38个电子,若XY2为常见元素形成的离子化合物,其电子式为:______________;若XY2为共价化合物时,其结构式为:__________________。
(3)氯化铝的物理性质非常特殊,如:氯化铝的熔点为190℃(2.02×103 Pa),但在180℃就开始升华,据此判断,氯化铝是________(填“共价化合物”或“离子化合物”),可以证明你的判断正确的实验依据是______________________________________________。
(4)现有a~g 7种短周期元素,它们在周期表中的位置如下,请据此回答下列问题:
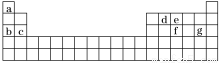
①元素的原子间反应最容易形成离子键的是________(填序号,下同),容易形成共价键的是______;
A.c和f B.b和g C.d和g D.b和e
②写出a~g 7种元素形成的所有原子都满足最外层为8电子结构的任意一种分子的分子式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com