
| 编号 | 电极材料 | 电解质溶液 | 电子流动 方向 |
| 1 | Mg-Al | 稀盐酸 | Mg流向Al |
| 2 | Mg-Al | NaOH溶液 |



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
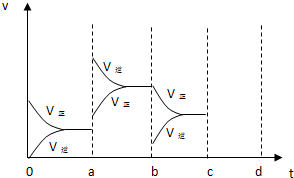
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | 30 | 30 | 30 | 30 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V2 | 20 |
| H2O/mL | 20 | 19.5 | V3 | 15 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③④ | B.②④⑥ | C.②⑤⑥ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③⑤ | B.①②④⑤ | C.①③④⑤ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数增大,乙中B的体积分数减小 |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com