
【题目】按要求完成下列填空:
(1)画出Mg原子结构示意图: , O2﹣结构示意图: .
(2)现有以下物质:①NaCl溶液;②Cu;③乙醇(C2H5OH);④熔融的KNO3;⑤BaSO4固体;⑥干冰.
其中:属于电解质的是;属于非电解质的是;能导电的是(以上都用序号填写).
(3)11.0g 由 ![]() 和
和 ![]() 组成的水分子,其中含中子数为mol,电子数为mol.
组成的水分子,其中含中子数为mol,电子数为mol.
(4)已知某植物营养液配方为0.3mol KCl,0.2mol K2SO4 , 0.1mol ZnSO4和1L水.若以KCl,K2SO4 , ZnCl2和1L水为原料配得相同组成的营养液,需三种溶质KClmol,K2SO4mol,ZnCl2mol.
【答案】
(1)![]() ;
;![]()
(2)④⑤;③⑥;①②④
(3)6;5
(4)0.1;0.3;0.1
【解析】解:(1)镁原子核外12个电子,分为三个电子层最外层为2个电子,Mg原子结构示意图: ![]() ,氧离子是氧原子得到2个电子形成的阴离子,核外两个电子层最外层8个电子O2﹣结构示意图:
,氧离子是氧原子得到2个电子形成的阴离子,核外两个电子层最外层8个电子O2﹣结构示意图: ![]() ,
,
所以答案是: ![]() ;
; ![]() ;(2)①NaCl溶液含有自由离子,能够导电;属于混合物,既不是电解质也不是非电解质;
;(2)①NaCl溶液含有自由离子,能够导电;属于混合物,既不是电解质也不是非电解质;
②Cu含有自由电子,能够导电;是单质,既不是电解质也不是非电解质;
③乙醇(C2H5OH)不含有自由电子或者自由移动的离子,不导电;在水溶液中和在熔融状态下都能导电,属于电解质;
④熔融的KNO3含有自由移动的离子,能导电;在水溶液中和在熔融状态下能导电,属于电解质;
⑤BaSO4固体不含有自由电子或者自由移动的离子,不导电;在熔融状态下能导电,属于电解质;
⑥干冰不含有自由电子或者自由移动的离子,不导电;本身不能电离产生自由移动离子,属于非电解质;
属于电解质的为④⑤,属于非电解质的为③⑥,能导电的为①②④;
所以答案是:④⑤、③⑥、①②④;(3)由21H和188O组成的水分子的相对分子质量为22,则11g的物质的量为 ![]() =0.5mol,其中含中子数为(2×1+18﹣8)×0.5mol=6mol,电子数为(2×1+8)×0.5mol=5mol,
=0.5mol,其中含中子数为(2×1+18﹣8)×0.5mol=6mol,电子数为(2×1+8)×0.5mol=5mol,
所以答案是:6;5;(4)解:0.3molKCl、0.2molK2SO4、0.1molZnSO4中,含有的各离子的物质的量为:
n(K+)=0.3mol+0.2mol×2=0.7mol,
n(Zn2+)=0.1mol,
n(Cl﹣)=0.3mol,
n(SO42﹣)=0.2mol+0.1mol=0.3mol,
所以需要需n(K2SO4)=0.3mol;
n(ZnCl2)=0.1mol;
n(KCl)=0.7mol﹣2×0.3mol=0.1mol,
根据锌离子守恒可知,需要n(ZnCl2)=0.1mol,此时也提供了Cl﹣0.2mol,再由SO42﹣守恒得n(K2SO4)=0.3mol,由Cl﹣守恒,则n(KCl)=0.3mol﹣0.2mol=0.1mol,
所以KCl、K2SO4、ZnCl2的物质的量各是0.1mol、0.3mol、0.1mol,
所以答案是:0.1,0.3,0.1.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】(2分)一定温度下,可逆反应2NO2![]() 2NO+O2,在体积固定的密闭容器中反应,达到平衡状态的标志是( )
2NO+O2,在体积固定的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2,同时生成2n mol NO2;
②单位时间内生成n mol O2,同时生成2n mol NO;
③NO2、NO、O2的浓度比为2:2:1;
④混合气体的压强不再改变;
⑤混合气体的颜色不再改变;
⑥混合气体的平均摩尔质量不再改变.
A. ①④⑤⑥ B. ①②③⑤ C. ②③④⑥ D. 以上全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() I是常规核裂变产物之一,可以通过测定大气或水中
I是常规核裂变产物之一,可以通过测定大气或水中 ![]() I的含量变化来检测核电站是否发生放射性物质泄漏.下列有关
I的含量变化来检测核电站是否发生放射性物质泄漏.下列有关 ![]() I的叙述中错误的是( )
I的叙述中错误的是( )
A.![]() I的化学性质与
I的化学性质与 ![]() I相同
I相同
B.![]() I的质子数为53
I的质子数为53
C.![]() I的原子核外电子数为78
I的原子核外电子数为78
D.![]() I的原子核内中子数多于质子数
I的原子核内中子数多于质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的下列溶液:HCl、H2SO4、CH3COOH,导电能力由强到弱的顺序是
A. HCl=H2SO4>CH3COOH B. HCl>H2SO4>CH3COOH
C. H2SO4>HCl>CH3COOH D. HCl=H2SO4=CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列化学用语:
(1)书写电离方程式:H2SO4:;NH4NO3: .
(2)从电子得失角度,用双线桥法分析下列氧化还原反应中化合价变化的关系,标出电子转移的方向和数目并配平氧化还原反应式:
K2Cr2O7+HCl=KCl+CrCl3+Cl2↑+H2O
氧化剂: , 被氧化的元素:;盐酸体现的性质是: .
(3)工业上用电解饱和食盐水制Cl2 , 写出化学反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
H2O(g) == H2(g) +1/2 O2(g) △H = +241.8 kJ·mol-1
H2(g)+ 1/2O2(g) == H2O(1) △H = -285.8 kJ·mol-1
当1g液态水变为水蒸气时,其热量变化是
A. 吸热88kJ B. 吸热2.44 kJ C. 放热2.44 kJ D. 吸热44 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲配制250mL0.1molL﹣1的H2SO4溶液,回答下列有关问题,有如下操作步骤:
①把量取好的浓H2SO4沿烧杯壁缓缓倒入盛有一定量水的小烧杯中,并用玻璃棒不断搅拌
②把①中所得溶液小心转入仪器A中
③继续向A中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入A中,并轻轻摇匀
⑤用玻璃塞将A塞紧,充分摇匀
请填写下列空白: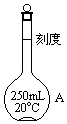
(1)写出图中仪器A的名称 , 使用此仪器A前应检查它是否 .
(2)操作步骤的正确顺序为(填序号) .
(3)转移溶液时,应先将溶液 , 然后将溶液沿玻璃棒注入仪器A中.
(4)若出现下列操作时,对所配溶液浓度将有何影响(填“偏高、偏低、无影响”)
①量筒用蒸馏水冼净后,再量取浓硫酸;
②不将洗涤液转移入仪器A就定容;
③定容时,仰视仪器A刻度线;
④仪器A只用蒸馏水洗涤,但未经干燥而配制溶液 .
(5)若实验过程中出现如下情况应如何处理?
①加蒸馏水时不慎超出了刻度;
②向容量瓶中转移溶液时,不慎有液滴掉在容量瓶外面 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL HNO3和H2SO4的混合溶液中,两种酸的物质的量浓度之和为0.6mol/L。向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大值为(反应前后溶液体积变化忽略不计)
A. 0.225mol/L B. 0.30mol/L C. 0.36mol/L D. 0.45mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com