
 按要求回答下列问题:
按要求回答下列问题:分析 (1)铝与氧化铁发生铝热反应生成氧化铝和铁,据此写出反应的化学方程式;该实验中除用到铝粉和Fe2O3外,需要的试剂还有氯酸钾和镁;
(2)①甲由具有相同电子层结构的阴、阳离子构成,则甲为Al2O3;灼烧得到的红棕色粉末1.60g应该是氧化铁,计算出氧化铁的物质的量,根据铁原子守恒可知铁的物质的量是及质量,从而得出合金中铝的质量,根据n=$\frac{m}{M}$计算出铝物质的量,就可以得出x:y;
②在加热的条件下氧化铝与氢氧化钠反应生成Na[Al(OH)]4;由于二氧化硅与能与氢氧化钠反应生成硅酸钠和水,所以含二氧化硅材料做成的坩埚不能用来熔融NaOH;
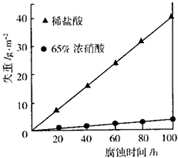
③结合图象可知乙在65%浓硝酸中具有比较强的抗腐蚀性,这是由于常温下遇浓硝酸表面钝化,阻碍进一步反应;
④Al4C3遇水会产生一种气体,则根据CaC2+2H2O═Ca(OH)2+C2H2↑可推测,Al4C3与水反应生成氢氧化铝和甲烷;
(3)1 mol Mg17Al12完全吸氢后可以吸收17mol氢气,因此释放时可以再释放出17mol氢气,同时镁和铝也分别都能与盐酸反应放出氢气;1 mol Mg17Al12中含有17mol镁、12mol铝,计算出铝和镁与盐酸反应生成的氢气的物质的量,便可得到1mol Mg17Al12完全吸氢后得到的混合物与上述盐酸完全反应,释放出H2的物质的量.
解答 解:(1)铝与氧化铁发生铝热反应的方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;该实验中除用到铝粉和Fe2O3外,需要的试剂还有氯酸钾和镁,故ab正确,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;ab;
(2)①甲由具有相同电子层结构的阴、阳离子构成,则甲是Al2O3;取该合金粉末2.47g,滴加足量浓NaOH溶液,其中铝溶解转化为偏铝酸钠,充分搅拌、过滤、洗涤得固体铁.再将所得固体在空气中充分加热、灼烧得红棕色粉末1.60g,所以红棕色粉末应该是氧化铁,物质的量为:$\frac{1.60g}{160g/mol}$=0.01mol;根据铁原子守恒可知铁的物质的量是0.02mol,质量是0.02mol×56g/mol=1.12g,因此合金中铝的质量是2.47g-1.12g=1.35g,物质的量为:$\frac{1.35g}{27g/mol}$=0.05mol,所以x:y=0.02:0.05=2:5,则x=2、y=5,
故答案为:Al2O3;2,5;
②在加热的条件下氧化铝与氢氧化钠反应,反应的化学方程式为:Al2O3+2NaOH+3H2O═2Na[Al(OH)]4;
二氧化硅与能与氢氧化钠反应生成硅酸钠和水,所以含二氧化硅材料做成的坩埚不能用来熔融NaOH,
故答案为:Al2O3+2NaOH+3H2O═2Na[Al(OH)]4;不能;
③根据图象可知乙在65%浓硝酸中具有比较强的抗腐蚀性,这是由于常温下遇浓硝酸表面钝化,阻碍进一步反应,
故答案为:65%浓硝酸;遇浓硝酸表面钝化,阻碍进一步反应(只要体现出“钝化”即可);
④Al4C3遇水会产生一种气体,则根据CaC2+2H2O═Ca(OH)2+C2H2↑可推测,Al4C3与水反应生成氢氧化铝和甲烷,因此该气体的分子式为:CH4,
故答案为:CH4;
(3)1 mol Mg17Al12完全吸氢后可以吸收17mol氢气,因此释放时可以再释放出17mol氢气,同时镁和铝也分别都能与盐酸反应放出氢气;1 mol Mg17Al12中含有17mol镁、12mol铝,与元素反应分别放出17mol氢气和12mol×$\frac{3}{2}$=18mol氢气,则得到的混合物与上述盐酸完全反应,释放出氢气的物质的量为:17mol+17mol+18mol=52mol,
故答案为:52mol.
点评 本题考查金属镁、铝、铁等有关性质与计算,题目难度中等,试题知识点较多、综合性较强,充分考查学生的分析、理解能力及化学计算能力,注意掌握铝热反应原理,明确常见金属单质及其化合物性质.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,10L pH=1的硫酸溶液中含有的H+数为NA | |
| B. | 将58.5g NaCl溶于1.00L水中,所得NaCl溶液的浓度为1.00mol•L-1 | |
| C. | 1molCl2与足量的铁反应,转移的电子数为3NA | |
| D. | 1molAl3+含有的核外电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D氢化物的稳定性比B氢化物的稳定性强 | |
| B. | 5种元素中,E元素氧化物的水合物的酸性最强 | |
| C. | A与B、D分别可形成AB2、AD2的化合物 | |
| D. | B和C可形成离子化合物,且C离子的半径大于B离子的半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋可除去热水壶内壁的水垢 | |
| B. | 淀粉,油脂 和蛋白质都是高分子化合物 | |
| C. | 服用铬含量超标的药用胶囊会对人对健康造成危害 | |
| D. | 新型复合材料使手机、电脑等电子产品更轻巧、实用和新潮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL 20mL | B. | 20mL 30mL | C. | 10mL 36.7mL | D. | 20mL 36.7mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol苯甲酸在浓H2SO4存在下与足量乙醇反应可得1 mol苯甲酸乙酯 | |
| B. | 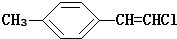 分子中的所有原子有可能共平面 分子中的所有原子有可能共平面 | |
| C. | 分子式为C5H12O的醇,能在铜催化下被O2氧化为醛的同分异构体有4种 | |
| D. | 1 mol阿司匹林(结构简式见图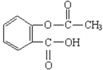 )与足量的氢氧化钠溶液加热反应,最多消耗的氢氧化钠的物质的量2 mol )与足量的氢氧化钠溶液加热反应,最多消耗的氢氧化钠的物质的量2 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com