
下列各项比较中前者高于(或大于或强于)后者的是
A、CCl4和SiCl4的熔点
B、邻羟基苯甲醛(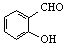 )和对羟基苯甲醛(
)和对羟基苯甲醛(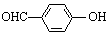 )的沸点
)的沸点
C、SO2和CO2在水中的溶解度
D、H2SO3和H2SO4的酸性
科目:高中化学 来源: 题型:
既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的方法是
A.通入足量溴的四氯化碳溶液中
B.与足量的液溴反应
C.通入酸性高锰酸钾溶液中
D.一定条件下与H2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学键的叙述,正确的是 ( )
A.离子化合物中一定含有离子键
B.单质分子中均不存在化学键
C.氯化氢和氯化钾溶解时破坏的化学键相同(2013·上海,4C改编)
D.含有共价键的化合物一定是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式:________。F的原子结构示意图为________。
(2)B、D形成的化合物BD2中存在的化学键为________键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为________化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为_________________________________________________。
(4)A、C、D、E的原子半径由大到小的顺序是________(用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性________于F(填“强”或“弱”),并用化学方程式证明上述结论____________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列微粒的个数比不是1∶1的是
A、NaCl晶体中阴、阳离子 B、NH3分子中的质子和电子
C、Na2O2固体中阴、阳离子 D、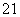 H原子中的质子和中子
H原子中的质子和中子
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了某短周期元素R的各级电离能数据(用I1、I2表示,单位为kJ·mol-1)。
| I1 | I2 | I3 | I4 | …… | |
| R | 740 | 1 500 | 7 700 | 10 500 | …… |
下列关于元素R的判断中一定正确的是
A、R的最高正价为+3价 B、R元素位于元素周期表中第ⅡA族
C、R元素的原子最外层共有4个电子 D、R元素基态原子的电子排布式为1s22s2
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z 单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
A、元素W 的简单气态氢化物的热稳定性比X 的强
B、元素W 的最高价氧化物对应水化物的酸性比Z 的弱
C、化合物YX、ZX2、WX3 中化学键的类型相同
D、原子半径的大小顺序: r(Y )>r(Z )>r(W) >r(X)
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9。单质Y和W都可与浓的NaOH溶液反应。下列说法不正确的是( )
A.原子半径:Y>Z>W
B.非金属性最强的元素为W
C.Y的最高价氧化物对应的水化物为强酸
D.XW2分子中各原子最外层电子均达到8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
用石墨电极电解100 mL H2SO4与CuSO4的混合溶液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
A.1 mol·L-1 B.2 mol·L-1C.3 mol·L-1 D.4 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com