
| A、Cl2>I2>Fe3+>SO2 |
| B、Cl2>Fe3++>I2>SO2 |
| C、Fe3+>Cl2>I2>SO2 |
| D、Cl2>Fe3+>SO2>I2 |


科目:高中化学 来源: 题型:
| A、AgCl沉淀生成和沉淀溶解不断进行,但速率相等 |
| B、AgCl难溶于水,溶液中没有Ag+和Cl- |
| C、在AgCl的澄清饱和溶液中,只要向其中加入NaCl溶液,一定会有沉淀生成 |
| D、向含有AgCl沉淀的悬浊液中加入NaCl固体,AgCl的溶解度增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
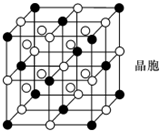 A,B,C,D,E,F都是短周期元素,原子序数依次增大,B,C同周期且相邻,A,D同主
A,B,C,D,E,F都是短周期元素,原子序数依次增大,B,C同周期且相邻,A,D同主x- 6 |
 表示)位于该正方体的顶点和面心.该化合物的化学式是
表示)位于该正方体的顶点和面心.该化合物的化学式是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C3H6、CH2=CHCH3 |
B、-OH、 |
C、 、 、 |
D、 、1s22s22p63s23p6 、1s22s22p63s23p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、约-40℃ |
| B、约-182℃ |
| C、约-108℃ |
| D、约56℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L的硫酸 |
| B、0.1mol/L的碳酸 |
| C、0.1mol/L的醋酸 |
| D、0.1mol/L的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠着火时,可用泡沫灭火器灭火 |
| B、蒸发结晶时应将溶液蒸干 |
| C、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| D、在氢氧化钠溶液中滴入氯化铁饱和溶液可以制得氢氧化铁胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C H3COOH与CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |
| B、常温下,0.1mol.L-1CH3COONa溶液和0.1mol.L-1NaHCO3溶液,NaHCO3溶液的pH大 |
| C、0.1mol.L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| D、将l mol KC1、l mol KHS溶于水配成的混合溶液中:n(K+)=n(S2-)+n(HS-)+n(H2S) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com