
下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
A.0.1 mol·L-1 Na2CO3溶液中:c(Na+)=c(HCO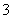 )+c(H2CO3)+2c(CO
)+c(H2CO3)+2c(CO )
)
B.常温下,pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7
C.将0.2 mol·L-1 NaA溶液和0.1 mol·L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)
D.pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等
【解析】 A项,在碳酸钠溶液中,物料守恒式:c(Na+)=2c(CO )+2c(HCO
)+2c(HCO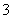 )+2c(H2CO3),A项错误;B项,常温下,Kw=1.0×10-14,pH=4的醋酸溶液中c(H+)=1.0×10-4mol·L-1,pH=10的氢氧化钠溶液中c(OH-)=1.0×10-4mol·L-1,由于醋酸是弱酸,其溶液中含有大量的CH3COOH,还会继续电离出H+,溶液呈酸性,B项正确;C项,由电荷守恒知c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(A-),C项错误;D项,氢氧化钡溶液中,Ba(OH)2===Ba2++2OH-,H2OH++OH-,溶液中氢离子来自水的电离,所以pH=12的氢氧化钡溶液中水电离的c(H+)=1.0×10-12mol·L-1,而碳酸钠溶液中存在CO
)+2c(H2CO3),A项错误;B项,常温下,Kw=1.0×10-14,pH=4的醋酸溶液中c(H+)=1.0×10-4mol·L-1,pH=10的氢氧化钠溶液中c(OH-)=1.0×10-4mol·L-1,由于醋酸是弱酸,其溶液中含有大量的CH3COOH,还会继续电离出H+,溶液呈酸性,B项正确;C项,由电荷守恒知c(H+)+c(Na+)=c(OH-)+c(Cl-)+c(A-),C项错误;D项,氢氧化钡溶液中,Ba(OH)2===Ba2++2OH-,H2OH++OH-,溶液中氢离子来自水的电离,所以pH=12的氢氧化钡溶液中水电离的c(H+)=1.0×10-12mol·L-1,而碳酸钠溶液中存在CO +H2OHCO
+H2OHCO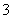 +OH-,OH-来自水电离,水电离的OH-浓度与H+浓度相等,所以pH=12的Na2CO3溶液中水电离的c(H+)=
+OH-,OH-来自水电离,水电离的OH-浓度与H+浓度相等,所以pH=12的Na2CO3溶液中水电离的c(H+)= mol·L-1=1.0×10-2mol·L-1,两溶液中水电离的氢离子浓度不相等,D项错误。
mol·L-1=1.0×10-2mol·L-1,两溶液中水电离的氢离子浓度不相等,D项错误。
【答案】 B


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
下列离子方程式中,属于水解反应的是( )
A.CH3COOH +H2O  CH3COO- + H3O+
CH3COO- + H3O+
B.SO2 + H2O  HSO3- + H+
HSO3- + H+
C.HS- + H2O  S2- + H3O+
S2- + H3O+
D.CO32- + H2O  HCO3- + OH-
HCO3- + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
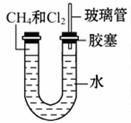 如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1∶4)的混合气体,假定氯气在水中的溶解度可以忽略。将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间。
如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1∶4)的混合气体,假定氯气在水中的溶解度可以忽略。将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间。
(1)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:___________。
(2)若题目中甲烷与氯气的体积比为1∶1,则得到的产物为_________ 。
A.CH3Cl HCl
B.CCl4 HCl
C.CH3Cl CH2Cl2
D.CH3Cl CH2Cl2 CHCl3 CCl4 HCl
(3)经过几个小时的反应后,U形管右端的水柱变化是_______ 。
A.升高 B.降低 C.不变 D.无法确定
(4)若水中含有Na2SiO3,则在U形管左端会观察____ 。
(5)右端玻璃管的作用是_________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)pH=13的CH3COONa溶液加水稀释100倍后,pH________11(填“>”“=”或“<”)原因是______________________________________________(用离子方程式和必要的文字说明);pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH________NaOH溶液的pH(填“>”“=”或“<”);
(2)pH相等时,①NH4Cl ②(NH4)2SO4 ③NH4HSO4三种溶液中c(NH )由大到小的顺序为________;
)由大到小的顺序为________;
(3)等体积、等浓度的氢氧化钠与醋酸混合后溶液呈________性,溶液中c(Na+)________c(CH3COO-)(填“>”“=”或“<”);pH=13的氢氧化钠与pH=1的醋酸等体积混合后溶液呈________性,溶液中c(Na+)________c(CH3COO-)(填“>”“=”或“<”);
(4)将物质的量浓度相同的盐酸与氨水混合后,溶液中的c(NH )=c(Cl-),则混合后溶液呈________性,盐酸的体积________氨水的体积(填“>”“=”或“<”);
)=c(Cl-),则混合后溶液呈________性,盐酸的体积________氨水的体积(填“>”“=”或“<”);
(5)NaHSO4在水中的电离方程式为NaHSO4===Na++H++SO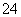 。该溶液中c(H+)_________________________c(OH-)+c(SO
。该溶液中c(H+)_________________________c(OH-)+c(SO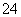 )(填“>”“=”或“<”)。
)(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
对可逆反应2A(s)+3B(g)  C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A的量,平衡向正反应方向移动 ②升高温度,平衡向逆反应方向移动,v(正)减小 ③压强增大一倍,平衡不移动,v(正)、v(逆)不变 ④增大B的浓度,v(正)>v(逆) ⑤加入催化剂,B的转化率提高
A.①② B.④ C.③ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
铜锌原电池(如右图)工作时,下列叙述正确的是
A.在外电路中,电流从Zn极流向Cu极
B.盐桥中的Cl-移向CuSO4溶液
C.当负极减小65g时,正极增加65g
D.电池的总反应为 Zn + Cu2+ = Zn2+ + Cu
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法中正确的是
A.标准状况下,11.2L Cl2和H2混合气体原子数为2NA
B.常温下,pH=1的H2SO4溶液中含有的H+的数目为0.2NA
C.在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA
D.标准状况下,2.24LCl2溶于水,转移的电子数目为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com