
分析 (1)钠的熔点较低,钠在加热条件下与氧气发生反应时,先熔化,与氧气在加热条件下反应生成淡黄色过氧化钠固体,燃烧时火焰为黄色,据此解答;
(2)Na2O2与H2O反应放出O2,将带火星的木条伸入试管中,木条复燃,证明生成的气体为O2;
(3)Na2O2与H2O反应生成NaOH和O2,不难推测出Na2O2与盐酸反应的化学方程式为2Na2O2+4HCl═4NaCl+2H2O+O2↑,而碱性氧化物是能与酸反应生成盐和水的氧化物,据此判断.
解答 解:(1)钠的熔点较低,钠在加热条件下与氧气发生反应时,先熔化,与氧气在加热条件下反应生成淡黄色过氧化钠固体,燃烧时火焰为黄色,
①钠熔点低,反应放热,金属钠熔成小球,故正确;
②在空气中燃烧,火焰为黄色,故错误;
③燃烧后生成产物为过氧化钠,为淡黄色,故错误;
④燃烧时火焰为黄色,故正确;
⑤燃烧后生成产物为过氧化钠,为淡黄色,故正确;
故选:C.
(2)Na在空气中加热得到的产物为淡黄色固体Na2O2,放入试管中,滴几滴水,Na2O2与H2O反应放出O2,化学方程式为2Na2O2+2H2O═4NaOH+O2↑,将带火星的木条伸入试管中,木条复燃,证明生成的气体为O2;故答案为:将带火星的木条伸入试管中,木条复燃则为O2;
(3)Na2O与H2O、盐酸反应的化学方程式分别为Na2O+H2O═2NaOH(生成碱)、Na2O+2HCl═2NaCl+H2O(生成盐和水),而Na2O2与H2O反应生成NaOH和O2,不难推测出Na2O2与盐酸反应的化学方程式为2Na2O2+4HCl═4NaCl+2H2O+O2↑,而碱性氧化物是能与酸反应生成盐和水的氧化物,而Na2O2与盐酸反应不只生成盐和水,还生成了O2,故Na2O2不属于碱性氧化物.
答案:2Na2O2+4HCl═4NaCl+2H2O+O2↑,不是碱性氧化物.
点评 本题考查了钠及其钠的氧化物的性质,注意钠在加热条件下能在空气中燃烧,但不加热时,生成氧化钠,题目难度不大,注意基础知识的积累.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ①⑥⑤③ | B. | ⑥③④③ | C. | ②③⑤③ | D. | ①③⑤③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
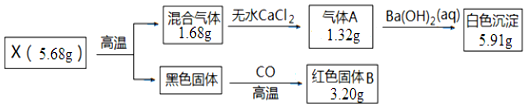
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
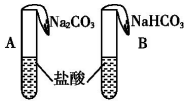 某学生在A、B两个装置的气球中分别装入1.06g Na2CO3和0.84g NaHCO3,试管中是足量的等浓度、等体积的盐酸,将两气球中物质同时倒入试管中完全反应.有关现象描述不正确的是(假设反应前后溶液体积不变)( )
某学生在A、B两个装置的气球中分别装入1.06g Na2CO3和0.84g NaHCO3,试管中是足量的等浓度、等体积的盐酸,将两气球中物质同时倒入试管中完全反应.有关现象描述不正确的是(假设反应前后溶液体积不变)( )| A. | 起初A气球鼓胀速度快,最终B气球大 | |
| B. | 起初B气球鼓胀速度快,最终两气球一样大 | |
| C. | 最终两溶液中氯离子物质的量浓度相同 | |
| D. | 最终两溶液中钠离子物质的量浓度不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.1 g由白磷和红磷组成的混合物中含有磷原子的数目为0.1NA | |
| B. | 0.1mol${\;}_{35}^{81}$Br原子中含中子数为3.5NA | |
| C. | 标准状况下,11.2LCHCl3中含有C-Cl键的数目为1.5NA | |
| D. | 0.5L1.0mol•L-1NH4Al(SO4)2溶液中含有的NH${\;}_{4}^{+}$数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液体分层,下层为苯层,黄色 | B. | 液体分层,下层为水层,紫色 | ||
| C. | 液体分层,上层为苯层,紫色 | D. | 液体分层,上层为水层,黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠的电子式: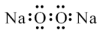 | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | NH4Cl的电子式: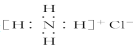 | D. | 硫原子的结构示意图: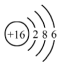 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1与0.2mol•L-1醋酸溶液,c(H+)之比 | |
| B. | 0.1mol•L-1Na2HPO4溶液,c(HPO42-)与c(Na+)之比 | |
| C. | pH=10的Ba(OH)2溶液与氨水,溶质的物质的量浓度之比 | |
| D. | pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com