
| A. | 所含氯元素的化合价越高,该物质的能量越高 | |
| B. | 所含氯元素的化合价越高,该物质越不稳定 | |
| C. | B→A+D的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO3-(aq)△H=-117kJ•mol-1 | |
| D. | ClO2-→ClO3-+ClO4-可以自发进行 |
分析 A、物质具有的能量越高越不稳定,根据图示信息来回答;
B、根据图物质具有的能量越高越不稳定,根据图示信息来回答
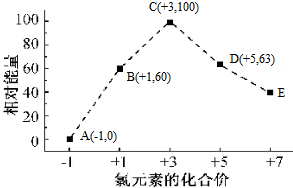
C、图示曲线可知Cl元素的化合价越来越高,由曲线可知D中Cl元素的化合价是+7价,因此ClOx-中x=4,即D为ClO3-,A为Cl-、B为ClO-,B→A+D的化学方程式为3ClO-=2Cl-+ClO3-,结合曲线可知ClO-相对Cl-的能量为60 kJ,ClO3-相对Cl-的能量为63 kJ,据此计算该反应的反应热;
D、根据歧化反应的规律和特点来回答判断.
解答 解:A、根据图示信息,氯元素的化合价越高,物质具有的能量先是升高后是降低,故A错误;
B、根据图示信息,氯元素的化合价越高,物质具有的能量先是升高后是降低,稳定性显示降低后是增强,故B错误;
C、图示曲线可知Cl元素的化合价越来越高,由曲线可知D中Cl元素的化合价是+7价,因此ClOx-中x=4,即D为ClO3-,A为Cl-、B为ClO-,B→A+D的化学方程式为3ClO-=2Cl-+ClO3-,结合曲线可知ClO-相对Cl-的能量为60 kJ,ClO3-相对Cl-的能量为63 kJ,因此该反应的反应热为△H=(63-60)kJ•mol-1-2×60 kJ•mol-1=-117 kJ•mol-1,故C正确;
D、ClO2-→ClO3-+ClO4-中氯元素的化合价从+3升高到了+5价和+7价,化合价只升高了,没有降低,所以以自发进行不能自发进行,故D错误.
故选C.
点评 本题是一道信息给定题,解体的关键是明确元素的化合价和微粒的能量之间的关系,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | A和B元素一定都是第二周期元素 | B. | A和B元素一定是同一主族元素 | ||
| C. | B元素可以是第二周期VIA族元素 | D. | A和B可以相互化合形成化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO4 | B. | HNO3 | C. | H2SO4 | D. | H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| a试管 | 紫色 | 蓝灰色 | 绿色 | 蓝灰色 |
| b试管 | 绿色 | 绿色 | 紫色 | 紫色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3、CO、CO2都是极性分子 | |
| B. | BF3、SiCl4都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、Hl的稳定性依次增强 | |
| D. | CS2、H2O、C2H2都是直线型分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应2NO2═N2O4在室温下可自发进行,则该反应的△H<0 | |
| B. | 工业上电解熔融态氯化铝冶炼单质铝 | |
| C. | CH3COOH 溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$的值增大 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH 减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com