用石墨做电极电解:①稀H2SO4 ②K2SO4溶液 ③CuCl2溶液 ④CuSO4 溶液 ⑤KOH溶液.
(1)阴阳极都有气体产生,且体积比(相同条件下)为2:1的是______(填序号,下同),其阳极的电极反应式都是______,阴极的电极反应式都是______,总反应的化学方程式是______ 2H2↑+O2↑
【答案】
分析:(1)电解水时,阴极氢离子放电,生成氢气,阳极氢氧根离子放电,生成氧气,两极都有气体产生,且体积比(相同条件下)为2:1;
(2)电解酸时,两极均有气体生成,溶液酸性增强,电解碱时,两极均有气体生成,溶液碱性增强;
(3)一个电极析出金属,一个电极析出气体,且溶液pH明显减小的是“放氧生酸型”的盐.
解答:解:(1)电解①②⑤时,阴极氢离子放电,生成氢气,即4H
++4e
-→2H
2↑,阳极氢氧根离子放电,生成氧气,
即4OH
-→O
2↑+2H
2O+4e
-,两极都有气体产生,且体积比(相同条件下)为2:1,
故答案为:①②⑤;4OH
-→O
2↑+2H
2O+4e
-;4H
++4e
-→2H
2↑;2H
2O

2H
2↑+O
2↑;
(2)电解①⑤时,阴极是氢离子得电子生成氢气,阳极是氢氧根离子失电子得到氧气,两极都有气体产生,①溶液的浓度增大,pH变小,⑤溶液的浓度增大,pH变大,故答案为:①;⑤;
(3)电解④是,阴极析出金属,阳极析出气体,且溶液中生成了酸,pH明显减小,
电解方程式为:2CuSO
4+2H
2O

2Cu+O
2↑+2H
2SO
4,
故答案为:④;2CuSO
4+2H
2O

2Cu+O
2↑+2H
2SO
4.
点评:本题考查学生电解池的工作原理知识,可以根据所学内容来回答,难度不大.

 2H2↑+O2↑;
2H2↑+O2↑; 2Cu+O2↑+2H2SO4,
2Cu+O2↑+2H2SO4, 2Cu+O2↑+2H2SO4.
2Cu+O2↑+2H2SO4.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案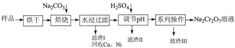
 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0gN2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧反应的热化学方程式是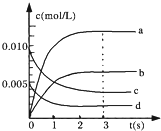 ( I)在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的交化如下表:
( I)在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的交化如下表: