
常温下,下列各组离子在指定的溶液中一定能大量共存的是
A.加入铝产生H2的溶液:NO3-、NH4+、Ba2+、Cl-、Na+
B.使酚酞变红的色的溶液:Na+、Cu2+、HCO3-、NO3-
C.0.1 mol/L的FeCl3溶液:Ba2+、NO3-、Na+、Cu2+、I-
D.0.1 mol/L的NH4Cl溶液:K+、Na+、HCO3-、SO42-
科目:高中化学 来源: 题型:
某课外实验小组设计的下列实验不合理的是( )
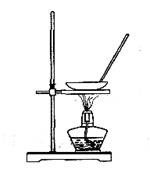
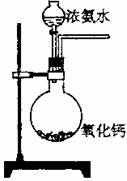
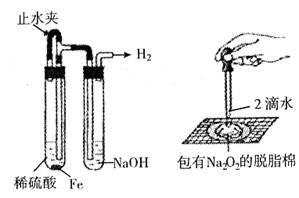
A. 蒸干NH4Cl饱和溶液制备NH4Cl晶体 B.实验室制备少量氨气
C.制备并观察氢氧化亚铁 D.证明过氧化钠与水反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号) 。
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式) 。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系
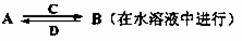
其中C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式 ;
D的电子式 。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为 ;
由A与过量的C反应转化为B的离子方程式 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因 。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.Na2S2O3溶液中加入稀盐酸:2S2O32-+2H+=SO42-+3S↓+H2O
B.磁性氧化铁溶于稀硝酸:3Fe3O4+28H++NO3- 9Fe3++NO↑+14H2O
9Fe3++NO↑+14H2O
C.100ml0.1mol/L FeI2溶液与标况下0.224L Cl2: 2Fe2++ Cl2=2Fe3++2Cl-
D.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:
2Al3++3SO42-+3Ba2++6OH -=2 Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
研究和开发CO2和CO的创新利用是环境保护和资源利用双赢的课题。
 (1)CO可用于合成甲醇。在体积可变的密闭容器
(1)CO可用于合成甲醇。在体积可变的密闭容器
中充入4molCO和8molH2,在催化剂作用下合成甲醇:
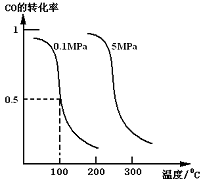
CO(g)+2H2(g) CH3OH(g)(Ⅰ),平衡时CO
CH3OH(g)(Ⅰ),平衡时CO
的转化率与温度、压强的关系如右图所示:
①该反应的逆反应属于________反应;(填“吸热”或
“放热”)。
②在0.1Mpa 、100℃的条件下,该反应达到平衡时容
器体积为开始容器体积的_________倍。(结果保留两位小数点)
③在温度和容积不变的情况下,再向平衡体系中充入4molCO,8molH2,达到平衡时CO转化率_______(填“增大”,“不变”或“减小”), 平衡常数K_______(填“增大”,“不变”或“减小”)。
(2)在反应(Ⅰ)中需要用到H2做反应物,以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+ H2O(g)= CO(g)+3H2(g) △H=+206.2 kJ·mol-1
CH4(g)+ CO2(g)= 2CO(g)+2H2(g) △H=+247.4 kJ·mol-1
则CH4和H2O(g)反应生成CO2和H2的热化学方程式为: 。
(3)在反应(Ⅰ)中制得的CH3OH 即可以做燃料,还可以与氧气组成碱性燃料电池,电解质溶液是20%~30%的KOH溶液。则该燃料电池放电时:负极的电极反应式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
amolFe与一定量的硝酸在一定条件下充分反应,将生成的气体与标准状况下b g O2混合,恰好能被水完全吸收,则a和b的关系可能是
A.0.5a≤b≤0.75a B.16a≤b≤24a C.0.2a≤b≤0.3a D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物X、Y、Z之间有如图所示的转化关系。下列说法中不正确的是
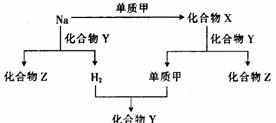
A.图中的每一步反应都是氧化还原反应
B.钠与Y物质的反应属于氧化还原反应但不是离子反应
C.X与Y的反应中,氧化剂和还原剂都是X
D.Z的水溶液能使酚酞试液变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学—选修2 化学与技术】
(15分) 高富氧底吹熔池炼铜新工艺反应炉如图

(1)该新工艺的优点之一是混合矿料不需要干燥、磨细。烟气进入余热锅炉后,经静电除尘后进入酸厂回收利用,这样做体现化学的________思想。
(2)该新工艺的优点之二是首次投料需要添加少量的燃料,当反应充分启动后就不需要再投放燃料,说明反应炉中的反应总体来说是________反应。
(3)此法冶炼的矿石主要是黄铜矿(主要成分是CuFeS2),经过上面设备煅烧后最终化合态的铜生成铜和SO2,在冶炼铜矿过程中存在重要反应:2CuFeS2+O2=Cu2S+2FeS+SO2、2Cu2S+3O2=2Cu2O+2SO2、________________________________。
(4)从放铜锍口放出的铜锍中还含有铁和硫必须除去,铜锍吹炼过程是火法冶炼生产粗铜的最后一道工序,吹炼过程分为两个阶段。第一阶段的任务是使铁氧化造渣,主要化学反应为:①2FeS+3O2+SiO2=2FeO·SiO2+2SO2 ,第二阶段是使上一个阶段中没有反应彻底的Cu2S氧化成粗铜,主要化学反应为:②Cu2S+O2=2Cu+SO2,下列关于反应①、②的分析正确的是________(填序号)
A.反应②氧化剂只有O2
B.硫元素在①和②均被氧化
C.①和②在反应过程中都有共价键破坏和共价键形成
(5)图中渣包中的炉渣含有Fe2O3、FeO 、SiO2等,选用提供的试剂设计实验验证炉渣中含有FeO。提供的试剂:KMnO4溶液、KSCN溶液、NaOH溶液、稀硫酸、稀盐酸,所选试剂为_______________。实验现象是__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
美丽的“水立方”是北京奥运会游泳馆,其建筑采用了膜材料ETFE,该材料为四氟乙烯与乙烯的共聚物。下列说法错误的是 ( )
A、四氟乙烯分子中既含有极性键又含有非极性键
B、ETFE分子中可能存在“-CH2-CH2-CF2-CF2-”的连接方式
C、ETFE在空气中易被氧化
D、ETFE是四氟乙烯和乙烯加聚反应的产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com